ГЛАВНАЯ ТЕМА: РАДИОФАРМАЦЕВТИЧЕСКИЕ ПРЕПАРАТЫ: НА ПУТИ К ПАЦИЕНТУ
Стратегия развития фармацевтической промышленности Российской Федерации на период до 2030 г. («Фарма-2030») содержит необходимые механизмы, которые позволят реализовать идею обеспечения технологической независимости Российской Федерации в области фармацевтической промышленности, в том числе в таком важном ее подразделе, как разработка, изучение и производство радиофармацевтических лекарственных препаратов. Своим видением о перспективах разработки, производства, регистрации и применения средств радионуклидной терапии в государствах — членах Евразийского экономического союза (ЕАЭС) делится начальник отдела координации работ в сфере обращения лекарственных средств и медицинских изделий Департамента технического регулирования и аккредитации Евразийской экономической комиссии кандидат медицинских наук Дмитрий Анатольевич Рождественский.
ВВЕДЕНИЕ. Радиофармацевтические лекарственные препараты (РФЛП) занимают важное место в современной ядерной медицине, являясь основой эффективных методов диагностики, терапии и тераностики онкологических заболеваний. Несмотря на быстрое развитие этой области, комплексный патентный анализ разработок отрасли, который позволил бы выявить ключевые направления научно-технического прогресса, определить лидеров рынка и оценить существующие риски и возможности, до настоящего времени остается недостаточно проработанным. Систематизация и анализ патентной активности в сфере РФЛП позволит не только отследить динамику развития технологий, но и выявить перспективные направления для дальнейших исследований и коммерциализации.
ЦЕЛЬ. Комплексный анализ патентной активности в радиофармацевтике для оценки ее современного состояния и выявления ключевых векторов технологического развития.
МАТЕРИАЛЫ И МЕТОДЫ. Исследование выполнено с использованием базы данных «Questel Orbit». Проанализированы 4988 патентных семейств за период 2000–2024 гг. с применением методов патентного и библиометрического анализа, сегментирования научно-технической информации. Критериями отбора служили индексы Международной патентной классификации и ключевые слова на русском и английском языках.
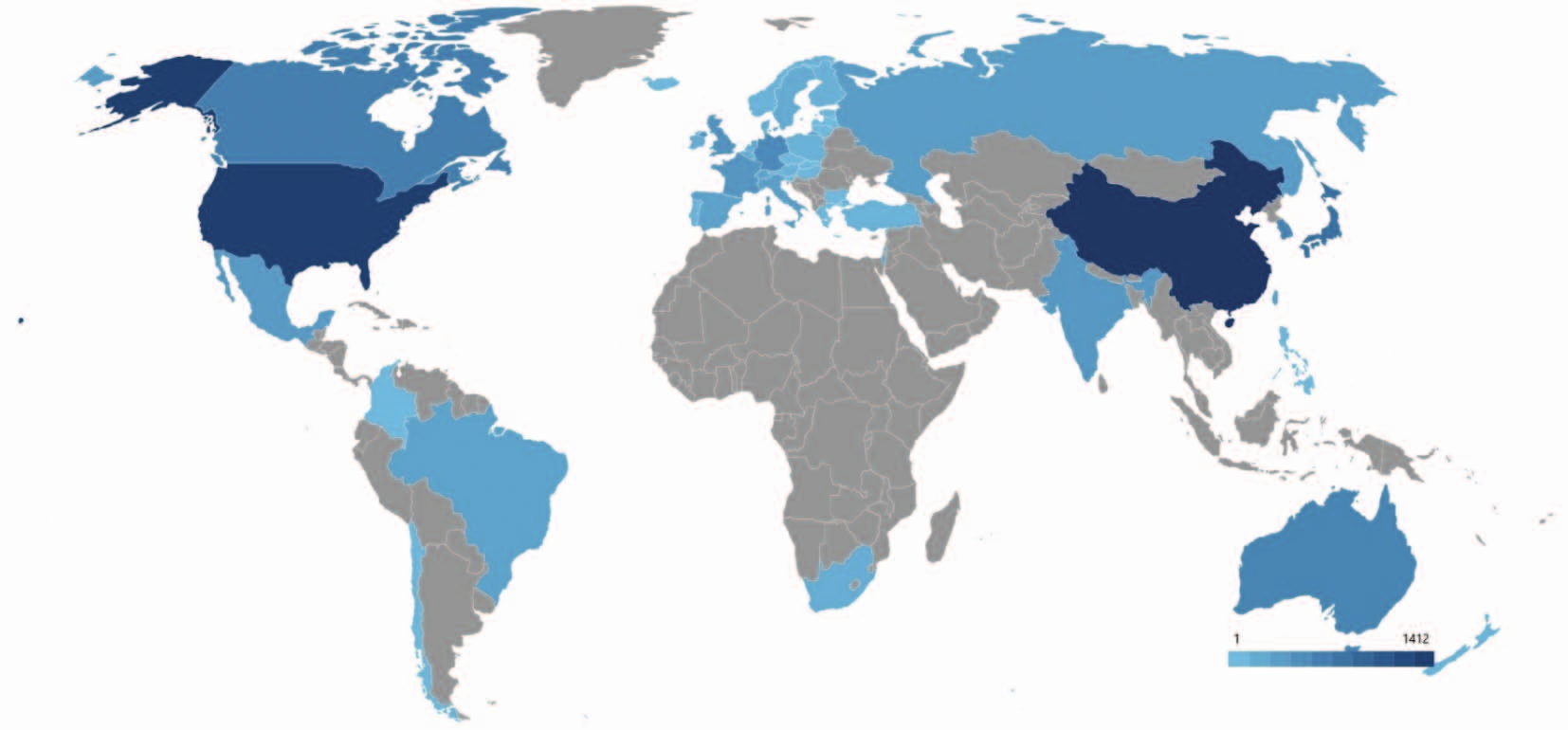
РЕЗУЛЬТАТЫ. Наблюдается рост патентной активности в мире после 2018 г., связанный с одобрением инновационных препаратов на основе 177Lu и 68Ga. Выделены три основных направления патентования и их доли в патентной базе: диагностика (43%), терапия (23%) и тераностика (34%). Лидерами в области патентования РФЛП выступают США, Китай и страны Европейского союза, обладающие развитой научно-технической базой и значительным коммерческим потенциалом. Определены различия в патентных стратегиях зарубежных и российских организаций. Зарубежные компании предпочитают использовать широкие формулы изобретений: в одном патенте они объединяют целый класс радионуклидов, несколько молекулярных носителей и способов доставки, что обеспечивает широкую правовую охрану и защищает инновации при незначительных изменениях состава препаратов. Такая стратегия позволяет комплексно охранять технологические разработки и создавать устойчивое конкурентное преимущество на рынке. В свою очередь, российские организации склонны оформлять более точечные патенты, ориентированные на конкретные технические решения. Это позволяет защищать отдельные инновации, но не обеспечивает такого широкого охвата и повышает риск обхода патентов конкурентами.
ВЫВОДЫ. Проведенный патентный анализ демонстрирует смещение фокуса научно-технических исследований с традиционных диагностических РФЛП в сторону комплексных тераностических РФЛП, объединяющих диагностические и терапевтические функции. Российская Федерация, несмотря на наличие практических разработок в сфере радиофармацевтики, значительно отстает в патентовании от обозначенных стран-лидеров. Кроме того, выявленная разница в подходах к написанию формул изобретений у зарубежных и российских исследователей и подходов к патентованию в целом подчеркивает необходимость совершенствования стратегий патентования изобретений в России с целью усиления охраны интеллектуальной собственности и стимулирования развития радиофармацевтической отрасли на международном уровне.
ВВЕДЕНИЕ. Потребность в новых решениях для диагностики и лечения широкого спектра заболеваний с использованием радиофармацевтических лекарственных препаратов (РФЛП), а также растущий рынок ядерной медицины стимулируют активную разработку и быстрый вывод в обращение инновационных РФЛП. Особенностью этого типа препаратов является наличие многокомпонентной структуры и специфической радиационной активности, что необходимо учитывать при планировании и контроле исследований по разработке препарата и дальнейшем трансфере технологий.
ЦЕЛЬ. Оптимизация процесса разработки РФЛП с помощью отраслевой шкалы уровней готовности технологии.
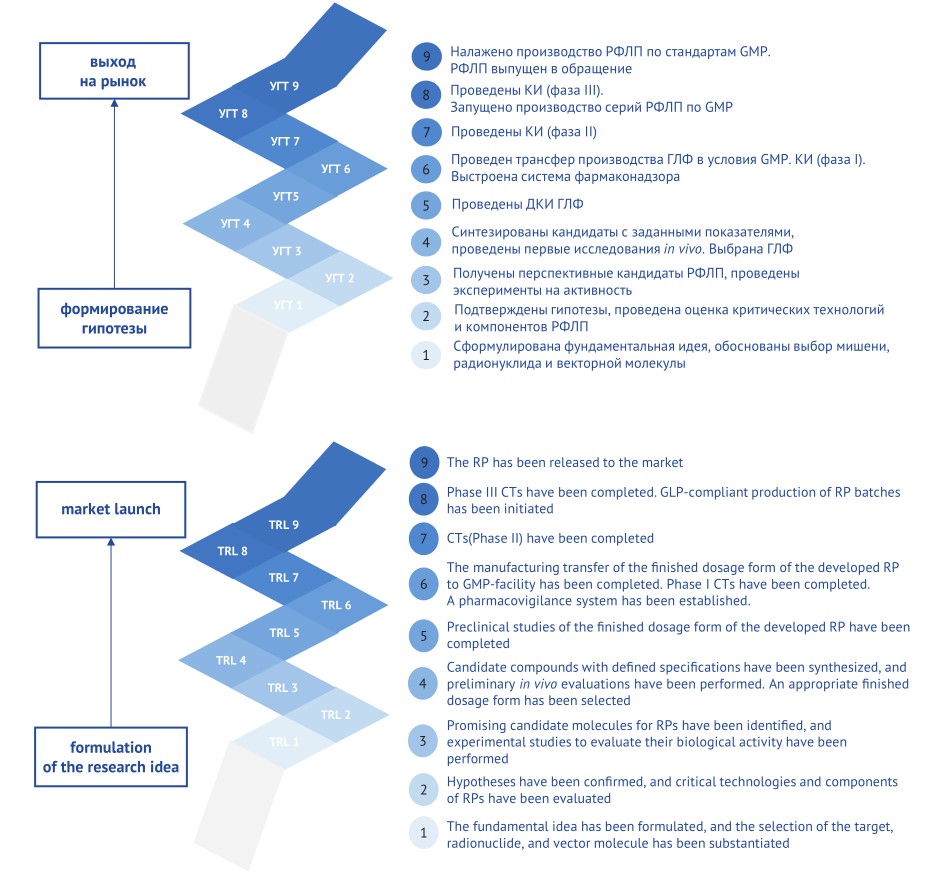
ОБСУЖДЕНИЕ. Рассмотрено применение отраслевой шкалы уровней готовности технологии РФЛП. Данная шкала учитывает ключевые особенности РФЛП: содержание в составе радиоактивного изотопа и биологической молекулы; необходимость контроля специфических показателей качества (радиохимической чистоты, стабильности и биологической активности), а также особенности обращения РФЛП на рынке. Критически важным является определение варианта применения и обращения разрабатываемого РФЛП, так как это определяет не только стратегию регистрации, но и требования к показателям качества получаемого препарата. На основании опыта АО «Росатом Наука» отмечены ключевые риски обращения (контаминация производственного оборудования, учет скорости радиоактивного распада при логистике и др.). Обсуждены особенности разработки воспроизведенных РФЛП (ускоренное прохождение первых четырех этапов разработки, необходимость подбора оригинальной молекулы-мишени), а также дизайн доклинических и клинических исследований для подтверждения биоэквивалентности воспроизведенного и референтного препаратов.
ВЫВОДЫ. Адаптированная шкала уровней готовности технологии РФЛП является инструментом, позволяющим комплексно контролировать ключевые этапы разработки, своевременно выявлять и минимизировать риски. Использование шкалы способствует ускорению вывода инновационных и воспроизведенных РФЛП на рынок за счет рутинного мониторинга процесса и поэтапного планирования полного цикла разработки, вплоть до стратегии обращения РФЛП на рынке.
ВВЕДЕНИЕ. Понятие «изготовление радиофармацевтических лекарственных препаратов (РФЛП)» в Российской Федерации было введено в Федеральном законе № 61-ФЗ «Об обращении лекарственных средств». За последние годы произошло существенное изменение законодательства в области производства и изготовления РФЛП. Сегодня стало возможным изготовление незарегистрированных РФЛП в медицинской организации для собственных нужд, что позволит быстро внедрять в клиническую практику новые методы и средства диагностики и лечения злокачественных новообразований, а также некоторых других заболеваний.
ЦЕЛЬ. Определение основных направлений развития ядерных аптек в Российской Федерации.
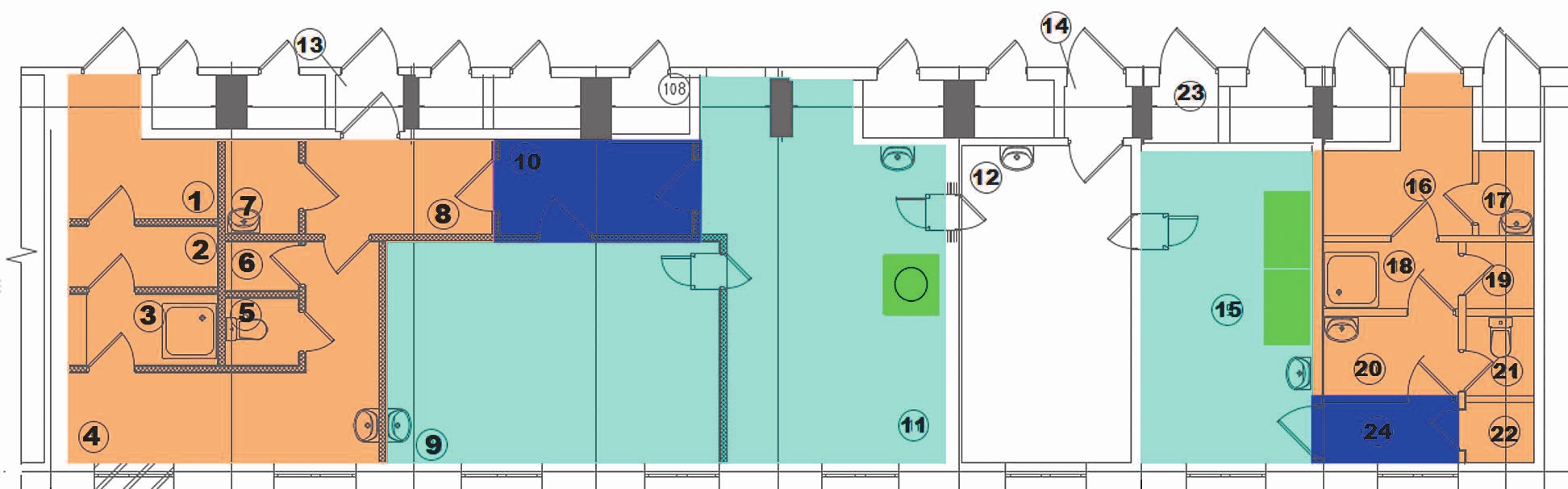
ОБСУЖДЕНИЕ. Термин «ядерная аптека» применяется к специальному подразделению медицинской организации, где проводится синтез и контроль качества РФЛП. Практика зарубежных госпитальных ядерных аптек доказала их преимущества в плане обеспечения наиболее короткого пути к пациентам жизненно необходимых препаратов. Проанализированы основные требования российских нормативных документов и рекомендаций, регламентирующих функционирование ядерной аптеки, а также опыт производственной ядерной аптеки РФЛП, созданной на базе Медицинского радиологического научного центра им. А.Ф. Цыба — Филиала Национального медицинского исследовательского центра радиологии Минздрава России. Регулярная работа ядерной аптеки позволяет принять на лечение незарегистрированными препаратами до нескольких сотен пациентов. Тем не менее в России практика организации ядерных аптек еще не стала рутинной и есть ряд задач, которые необходимо решить для эффективного функционирования таких аптек: создание системы подготовки специалистов-радиофармацевтов, определение объема предварительных исследований РФЛП, изготавливаемых экстемпорально в аптеке, внесение дополнений и корректировок в документацию по радиационной безопасности, регламентирующую порядок начала работ с новыми радионуклидами в условиях аптеки и др.
ВЫВОДЫ. Сложившаяся мировая практика функционирования госпитальных ядерных аптек доказала целесообразность существования такой формы обращения РФЛП. Подходы к изготовлению РФЛП за рубежом определяются национальным и региональным законодательством. Производственная аптека с правом изготовления РФЛП — новый вид аптечной организации, ранее не существовавший на территории государств — членов ЕАЭС. При формировании регуляторной базы аптечного изготовления РФЛП в России целесообразно учесть элементы мирового опыта, показавшие максимальную эффективность. Первоочередными задачами, которые необходимо решить, являются подготовка специализированного персонала, пересмотр ряда документов по радиационной безопасности, создание консультативной экспертной группы для подготовки решений по организационным и техническим вопросам развития ядерных аптек, определение источников финансирования лечения с применением изготовленных РФЛП.
ВВЕДЕНИЕ. Основанная на принципах управления рисками общая стратегия контроля содержания элементных примесей в лекарственных средствах, отраженная в монографиях национальных и мировых фармакопей, не распространяется на радиофармацевтические лекарственные препараты (РФЛП). Перечень нормируемых элементов и их пределы содержания в РФЛП определяет и обосновывает производитель.
ЦЕЛЬ. Разработка стратегии контроля содержания элементных примесей в РФЛП на основе сравнительного анализа требований национальных и мировых фармакопей к нормированию содержания элементных примесей в данном виде лекарственных средств.
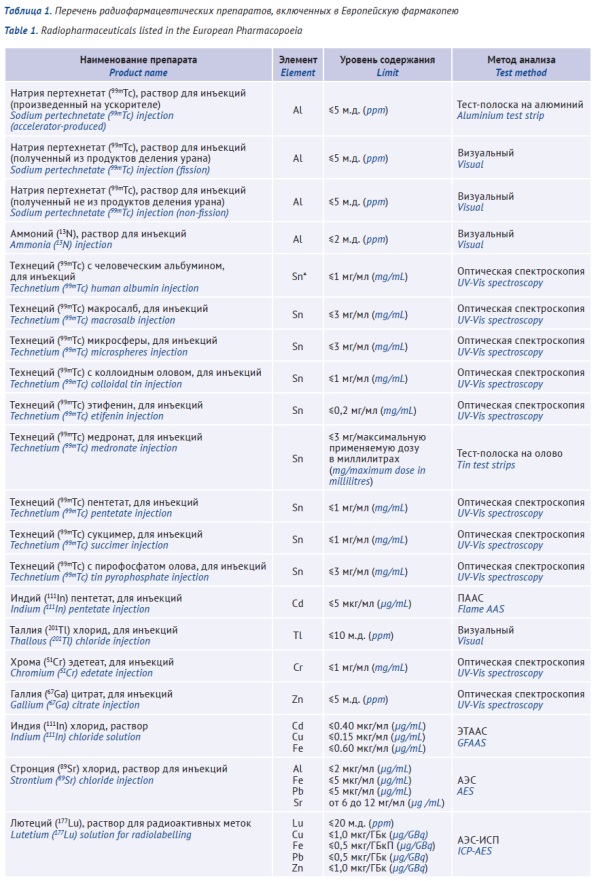
ОБСУЖДЕНИЕ. Пределы содержания элементных примесей в конкретных РФЛП приведены в частных монографиях фармакопей (24 монографии в Европейской фармакопее, по 7 в Индийской фармакопее и Государственной фармакопее Российской Федерации, по 6 в Фармакопеях США, КНР, Японии, 4 в Фармакопее Республики Корея). Монографии на одни и те же РФЛП различаются перечнем нормируемых элементов или пределами их содержания, общие критерии их выбора отсутствуют. В большинстве случаев нормируют содержание исходных нерадиоактивных элементов; элементов, соединения которых вводят в качестве стабилизаторов для задержки радиолиза или сорбентов (оксиды Ti, Zr, Sn и Al); элементов, снижающих эффективность радиоактивного мечения препарата (Cu, Fe, Pb, Zn в растворе 177Lu; Cu, Cd, Fe в растворе 111InCl; Cd, Cu, Fe, Pb, Zn в растворе 90Y и т.д.). Пределы содержания элементных примесей в РФЛП рассчитывают исходя из их допустимого воздействия на физико-химические, биологические и радиохимические свойства РФЛП с учетом дозы введения препарата. Содержание элементов с неустановленными значениями предельно допустимого суточного воздействия подлежит нормированию в том случае, если они оказывают влияние на процесс радиомечения препарата или целевого диагностируемого органа. В отношении прекурсоров РФЛП также отсутствует единый подход к нормированию содержания элементных примесей.
ВЫВОДЫ. Производителям РФЛП предложена стратегия контроля содержания элементных примесей в готовой продукции, основанная на оценке рисков их негативного влияния на качественные характеристики препарата. Она содержит обобщенные критерии выбора перечня нормируемых элементов и пределов их содержания в РФЛП, что существенно упрощает процесс подготовки нормативной документации по этому показателю.
ВВЕДЕНИЕ. Оценка производителями радиофармацевтических лекарственных препаратов (РФЛП) рисков негативного воздействия элементных примесей на качество своей продукции должна основываться на реальной информации об уровне элементной контаминации РФЛП. Накопление знаний о лекарственном препарате и процессе производства должно происходить начиная со стадии разработки и продолжаться на этапе его реализации вплоть до момента снятия лекарственного препарата с производства.
ЦЕЛЬ. Мониторинг содержания элементных примесей в РФЛП отечественных производителей методом масс-спектрометрии с индуктивно-связанной плазмой.
МАТЕРИАЛЫ И МЕТОДЫ. В качестве объектов исследования использовали 127 образцов различных РФЛП российских производителей, полученных ФГБУ «Научный центр экспертизы средств медицинского применения» в ходе уставной деятельности: флудезоксиглюкоза (18F), ПСМА-1007 (18F), натрия йодид (131I), натрия йодогиппурат (131I), йобенгуан (123I), натрия пертехнетат (99mTc). Содержание элементов Ag, Al, As, Au, Ba, Be, Bi, Cd, Co, Cr, Cu, Fe, Ga, Ge, Hg, Ir, Li, Mn, Nb, Ni, Os, Pb, Pd, Pt, Rh, Ru, Sb, Se, Mo, Sn, Tl, V, W, Zn определяли на масс-спектрометре Agilent 7900 по методике МУК 4.1.1483-03.
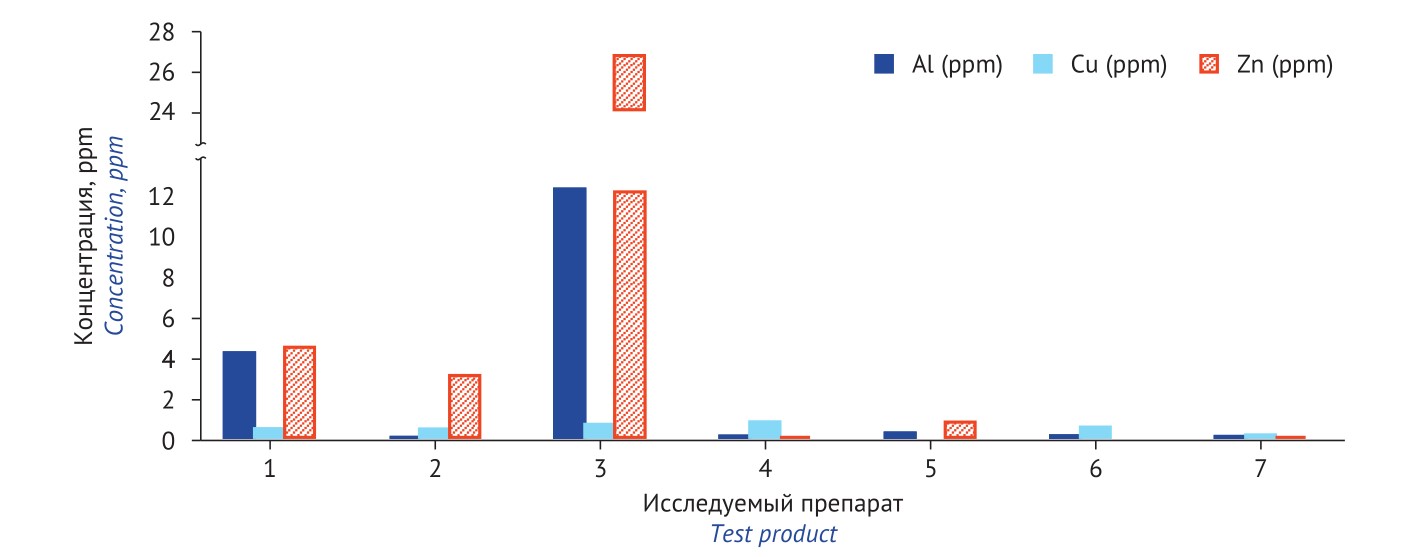
РЕЗУЛЬТАТЫ. Элементные примеси Ag, As, Au, Bi, Be, Cd, Co, Cr, Ga, Ge, Hg, Ir, Mo, Nb, Ni, Os, Pb, Pd, Pt, Rh, Ru, Sb, Se, Sn, Tl, V, W не обнаружены ни в одном из анализируемых РФЛП. Практически во всех проанализированных РФЛП максимальный уровень в элементную контаминацию вносят Al, Zn, Cu. В РФЛП для однофотонной эмиссионной компьютерной томографии (ОФЭКТ) содержится значительно меньше элементных примесей по сравнению с РФЛП для позитронно-эмиссионной томографии (ПЭТ).
ВЫВОДЫ. Элементы, вносящие максимальный вклад в контаминацию отечественных РФЛП (Al, Zn, Cu), являются нетоксичными или малотоксичными. Контроль над ними необходим в том случае, если они оказывают негативное влияние на качество РФЛП. Во флудезоксиглюкозе (18F) уровень элементной контаминации существенно зависит от используемого буферного раствора. Для точного понимания источников элементной контаминации исследованных РФЛП необходимо проведение дополнительного анализа элементных примесей исходных материалов, реактивов и полупродуктов на всех стадиях технологического процесса.
ВВЕДЕНИЕ. Производители отечественных радиофармацевтических лекарственных препаратов обязаны в ходе разработки и валидации производственного процесса определять в своей продукции содержание примесей Pb, As, Fe, а также других элементов, вносящих максимальный вклад в контаминацию препарата. На стадии предварительного мониторинга установлено, что такими элементами в препарате «Флудезоксиглюкоза (18F)» являются Al, Cu, Zn.
ЦЕЛЬ. Разработка и валидация методики определения содержания элементов Al, As, Cu, Fe, Pb, Zn в флудезоксиглюкозе (18F) методом масс-спектрометрии с индуктивно связанной плазмой.
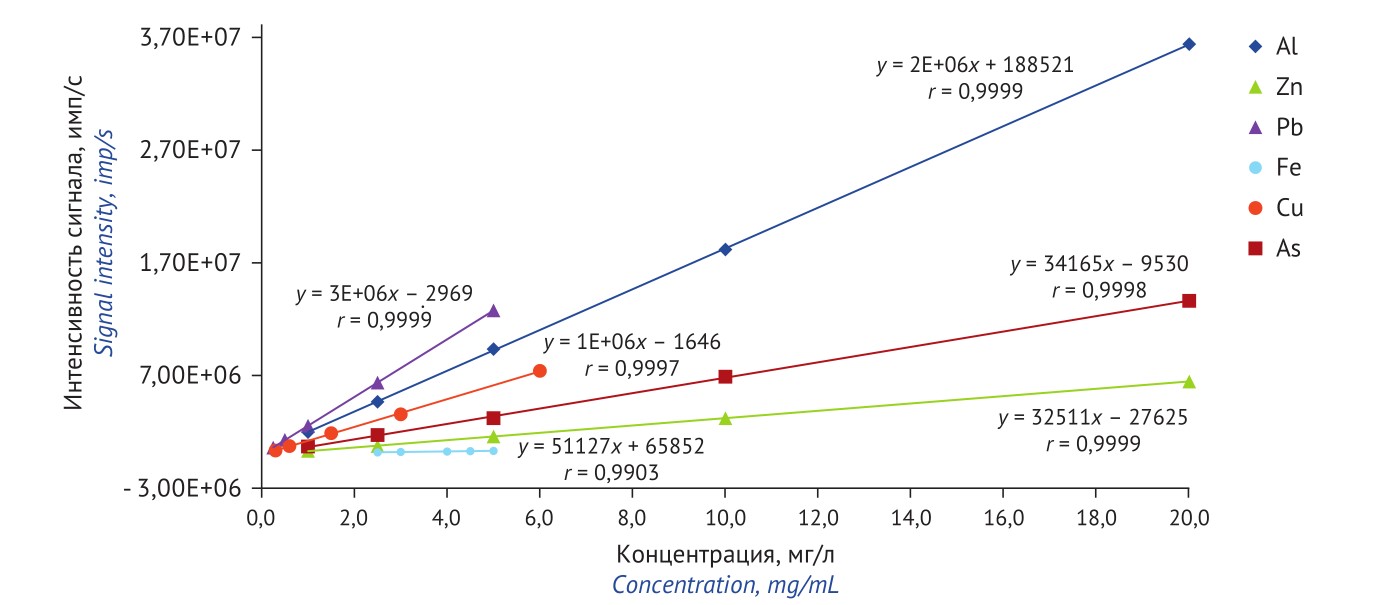
МАТЕРИАЛЫ И МЕТОДЫ. Разработку методики проводили на модельной смеси, имитирующей состав флудезоксиглюкозы (18F). Для валидации использовали образец препарата с минимальным содержанием анализируемых примесей, к которому добавляли варьируемые количества стандартных растворов определяемых элементов. Содержание элементов определяли на масс-спектрометре Agilent 7900. Фиксировали интенсивность сигналов следующих изотопов (а.е.м.): 27Al, 57Fe, 63Cu, 66Zn, 75As, 208Pb.
РЕЗУЛЬТАТЫ. Установлено, что органическая матрица не оказывает существенного влияния на результат элементного анализа. NaCl из-за матричного эффекта понижает открываемость элементов Al, Cu, Pb, Zn до уровня ниже 70%. При разбавлении модельной смеси в 10 раз открываемость анализируемых элементов составляет 90–101%. Коэффициенты корреляции линейных зависимостей «концентрация элемента — интенсивность сигнала» выше 0,99. Значения относительного стандартного отклонения (RSD) при оценке прецизионности не превышают 10%.
ВЫВОДЫ. Разработана методика определения содержания Al, As, Cu, Fe, Pb, Zn в флудезоксиглюкозе (18F) методом масс-спектрометрии с индуктивно связанной плазмой, учитывающая на стадии пробоподготовки влияние компонентов матрицы на количественную оценку целевых элементов. Валидационные характеристики методики соответствуют фармакопейным требованиям.
ЭКСПЕРТНОЕ МНЕНИЕ
ВВЕДЕНИЕ. Радиофармацевтические лекарственные препараты (РФЛП) применяются в современной клинической практике для диагностики и лечения широкого спектра заболеваний, при этом в нормативных актах Евразийского экономического союза (ЕАЭС) отсутствуют детализированные требования к данным раздела клинической документации регистрационного досье в форме общего технического документа, необходимого для оценки эффективности и безопасности этой группы препаратов.
ЦЕЛЬ. Определение прозрачных принципов формирования клинических разделов регистрационных досье различных типов и видов РФЛП, основанных на изучении положений действующей законодательной базы ЕАЭС, рекомендациях международных регуляторных органов и экспертном опыте.
ОБСУЖДЕНИЕ. Регистрация лекарственных препаратов по процедурам ЕАЭС и приведение регистрационных досье на препараты, зарегистрированные по национальной процедуре, в соответствие с требованиями ЕАЭС с расширением географии (включением стран признания) связаны с необходимостью предоставления полного регистрационного досье, включая модуль 5 «Клинические исследования». РФЛП обладают комплексом специфических свойств, связанных как с природой этих препаратов, так и со сферой их применения в клинической практике. Данные свойства РФЛП должны быть приняты во внимание при формировании стратегии разработки препарата (фармацевтической, доклинической и клинической), надлежащим образом изучены и описаны в документах регистрационного досье. Проведен анализ существующих регламентирующих документов ЕАЭС, а также рекомендаций регуляторных органов: Швейцарского агентства по лекарственным средствам (Swissmedic) и Министерства здравоохранения Канады (Health Canada), содержащих требования к клинической разработке РФЛП. Сформулированы правила формирования досье заявленных на регистрацию РФЛП в зависимости от их типа/вида и предполагаемого клинического применения.
ВЫВОДЫ. Описанные подходы к формированию досье для различных типов/ видов РФЛП могут помочь разработчикам и специалистам по регистрации в строгом исполнении регуляторных процедур.
ФАРМАКОПЕЯ
ВВЕДЕНИЕ. Масла жирные растительные широко используются в современной фармацевтической практике. В зависимости от способа получения и очистки они применяются для медицинских целей в качестве активной фармацевтической субстанции и (или) в качестве вспомогательного вещества. Метод получения масла и способ его очистки определяют требования к качеству и номенклатуре масел жирных растительных.
ЦЕЛЬ. Гармонизация национальных стандартов качества масел жирных растительных с требованиями ведущих мировых фармакопей.
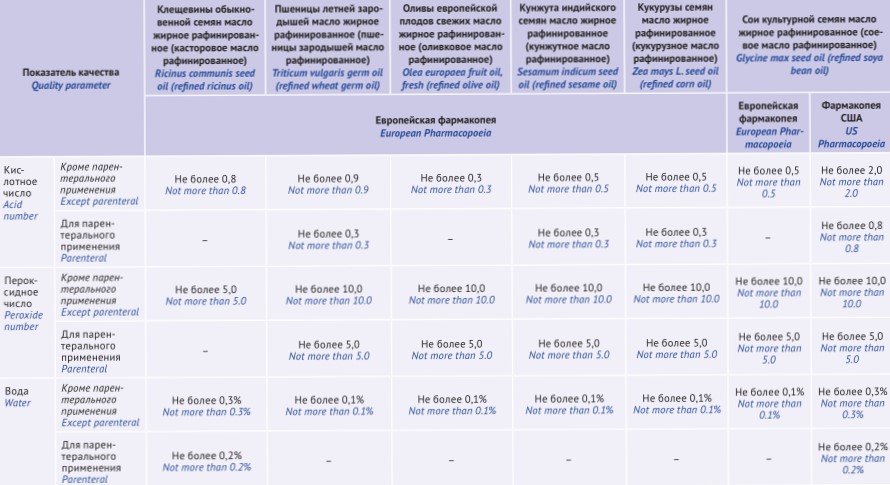
ОБСУЖДЕНИЕ. Актуальным направлением в решении вопросов стандартизации препаратов, содержащих биологически активные соединения, является сближение требований общих фармакопейных статей (ОФС) и фармакопейных стандартов ведущих мировых фармакопей, а также региональной Фармакопеи ЕАЭС. Сравнительный анализ ведущих мировых фармакопей показал, что в монографиях Европейской и Британской фармакопей предусмотрены классификация, методы получения и очистки масел жирных растительных. Очистка позволяет получить масла определенного качества, допускающего их использование, для производства лекарственных препаратов для парентерального применения. В отличие от монографий Европейской и Британской фармакопей, включающих только методы получения и очистки, Японская фармакопея и Фармакопея США предусматривают методы идентификации и испытания, которые могут быть применимы для масел жирных растительных.
ВЫВОДЫ. Анализ монографий ведущих мировых фармакопей позволил предложить проект ОФС «Масла жирные растительные», гармонизированный с требованиями аналогичных фармакопейных стандартов ведущих мировых фармакопей. Единый подход к требованиям предусматривает включение в ОФС классификации масел в зависимости от способа их получения и очистки, что влияет на показатели качества масла и его дальнейшее применение в медицинских целях. Учтены более жесткие требования к маслам, если они предназначены для производства парентеральных лекарственных препаратов, что указывается в соответствующих фармакопейных статьях.
РАЗРАБОТКА ЛЕКАРСТВЕННЫХ СРЕДСТВ
ВВЕДЕНИЕ. Ключевое влияние на планирование разработки оригинальных лекарственных препаратов оказывают крупнейшие зарубежные фармацевтические компании. Для определения направлений развития разработки оригинальных препаратов в России актуален анализ мировых трендов и слабых сигналов (тенденций) — ранних индикаторов значимых в будущем инноваций.
ЦЕЛЬ. Выявление трендов и тенденций, способных оказать влияние на фармацевтическую разработку в России, путем анализа спектра разрабатываемых оригинальных препаратов крупнейшими зарубежными компаниями.
МАТЕРИАЛЫ И МЕТОДЫ. Проведен анализ планов разработки препаратов на 2024 г. 20 крупнейших на мировом рынке зарубежных фармацевтических компаний, имеющих наиболее высокие бюджеты на исследования и разработки. Проанализированы оригинальные препараты, запланированные к изучению в клинических исследованиях I фазы за период январь — май 2024 г. Применена концепция описательного исследования, которая базируется на ретроспективном анализе вторичных данных. Измерениями проведенного анализа являлись номенклатура разрабатываемых оригинальных препаратов, направления разработки, целевые классы, виды и группы препаратов. На основании количественной и качественной оценки проводилось определение трендов и тенденций (слабых сигналов) в разработке оригинальных препаратов.
РЕЗУЛЬТАТЫ. За анализируемый период 17 из 20 крупнейших фармацевтических компаний включили в исследования I фазы 84 оригинальных препарата. Больше всего разрабатываемых молекул определено в направлениях: «онкология», «эндокринология и обмен веществ», «сердечно-сосудистая система», «иммунология». 40 препаратов включены в исследования I фазы в направлении «онкология». Наибольшее количество препаратов (42%) относится к молекулам с относительно высокой молекулярной массой. На основании выявленного количества препаратов у нескольких разработчиков сделано предположение о наличии трендов разработки для следующих классов: «Большая молекула» — биспецифическое антитело (10 препаратов, 5 разработчиков); моноспецифическое антитело (8 препаратов, 7 разработчиков); конъюгат «антитело — лекарственное средство» (8 препаратов, 3 разработчика); «Малая молекула» — ингибиторы ферментов (9 препаратов, 6 разработчиков); «Препарат клеточной терапии» — препараты на основе CAR-T технологии (6 препаратов, 2 разработчика).
ВЫВОДЫ. Актуальными трендами в развитии таргетной терапии является разработка биспецифических антител и конъюгатов «антитело–лекарство» нового поколения, параллельно с разработкой САR-T препаратов на основе аутологичных Т-клеток, преимущественно для терапии злокачественных новообразований. Исследование препаратов группы мультиспецифических антител формирует тенденцию разработки препаратов для таргетной терапии рака. Создание низкомолекулярных ингибиторов ферментов определяет тренд разработки препаратов в различных терапевтических областях. Разработка ингибиторов ферментов, воздействующих на мишени, основанные на принципе синтетической летальности (такие как WRN и PRMT5), является тенденцией в разработке малых молекул для прицельной терапии злокачественных опухолей.
ISSN 3034-3453 (Online)