Перейти к:
Анализ глобальных трендов патентования в радиофармацевтике: диагностика, терапия и тераностика
https://doi.org/10.30895/1991-2919-2025-15-4-377-390
Резюме
ВВЕДЕНИЕ. Радиофармацевтические лекарственные препараты (РФЛП) занимают важное место в современной ядерной медицине, являясь основой эффективных методов диагностики, терапии и тераностики онкологических заболеваний. Несмотря на быстрое развитие этой области, комплексный патентный анализ разработок отрасли, который позволил бы выявить ключевые направления научно-технического прогресса, определить лидеров рынка и оценить существующие риски и возможности, до настоящего времени остается недостаточно проработанным. Систематизация и анализ патентной активности в сфере РФЛП позволит не только отследить динамику развития технологий, но и выявить перспективные направления для дальнейших исследований и коммерциализации.
ЦЕЛЬ. Комплексный анализ патентной активности в радиофармацевтике для оценки ее современного состояния и выявления ключевых векторов технологического развития.
МАТЕРИАЛЫ И МЕТОДЫ. Исследование выполнено с использованием базы данных «Questel Orbit». Проанализированы 4988 патентных семейств за период 2000–2024 гг. с применением методов патентного и библиометрического анализа, сегментирования научно-технической информации. Критериями отбора служили индексы Международной патентной классификации и ключевые слова на русском и английском языках.
РЕЗУЛЬТАТЫ. Наблюдается рост патентной активности в мире после 2018 г., связанный с одобрением инновационных препаратов на основе 177Lu и 68Ga. Выделены три основных направления патентования и их доли в патентной базе: диагностика (43%), терапия (23%) и тераностика (34%). Лидерами в области патентования РФЛП выступают США, Китай и страны Европейского союза, обладающие развитой научно-технической базой и значительным коммерческим потенциалом. Определены различия в патентных стратегиях зарубежных и российских организаций. Зарубежные компании предпочитают использовать широкие формулы изобретений: в одном патенте они объединяют целый класс радионуклидов, несколько молекулярных носителей и способов доставки, что обеспечивает широкую правовую охрану и защищает инновации при незначительных изменениях состава препаратов. Такая стратегия позволяет комплексно охранять технологические разработки и создавать устойчивое конкурентное преимущество на рынке. В свою очередь, российские организации склонны оформлять более точечные патенты, ориентированные на конкретные технические решения. Это позволяет защищать отдельные инновации, но не обеспечивает такого широкого охвата и повышает риск обхода патентов конкурентами.
ВЫВОДЫ. Проведенный патентный анализ демонстрирует смещение фокуса научно-технических исследований с традиционных диагностических РФЛП в сторону комплексных тераностических РФЛП, объединяющих диагностические и терапевтические функции. Российская Федерация, несмотря на наличие практических разработок в сфере радиофармацевтики, значительно отстает в патентовании от обозначенных стран-лидеров. Кроме того, выявленная разница в подходах к написанию формул изобретений у зарубежных и российских исследователей и подходов к патентованию в целом подчеркивает необходимость совершенствования стратегий патентования изобретений в России с целью усиления охраны интеллектуальной собственности и стимулирования развития радиофармацевтической отрасли на международном уровне.
Ключевые слова
Для цитирования:
Аникеева М.Ю., Александров Ю.Д., Горбунова Ю.А., Попов Н.В., Кошевенко А.С., Иващенко В.В., Иванова Д.С., Николаева Е.Д., Степанова А.В., Федорова Д.И. Анализ глобальных трендов патентования в радиофармацевтике: диагностика, терапия и тераностика. Регуляторные исследования и экспертиза лекарственных средств. 2025;15(4):377-390. https://doi.org/10.30895/1991-2919-2025-15-4-377-390
For citation:
Anikeeva M.Yu., Aleksandrov Yu.D., Gorbunova Yu.A., Popov N.V., Koshevenko A.S., Ivashchenko V.V., Ivanova D.S., Nikolaeva E.D., Stepanova A.V., Fedorova D.I. Analysis of Global Patenting Trends in Radiopharmaceutical Industry: Diagnostics, Therapy, and Theranostics. Regulatory Research and Medicine Evaluation. 2025;15(4):377-390. (In Russ.) https://doi.org/10.30895/1991-2919-2025-15-4-377-390
ВВЕДЕНИЕ
Профилактика, выявление и терапия онкологических заболеваний являются одними из наиболее важных задач медицины как в России, так и за рубежом. Ученые по всему миру ведут интенсивные исследования, разрабатывая новые подходы к лечению и диагностике таких заболеваний.
В 2025 г. в Российской Федерации начата реализация национального проекта «Продолжительная и активная жизнь». В состав проекта вошел блок «Ядерная медицина». В рамках проекта планируется расширение инфраструктуры ядерной медицины для более точной диагностики на оборудовании нового поколения. Опорными учреждениями станут научные центры, которые ведут фундаментальные исследования в этом направлении1.
Активная разработка и внедрение в практику новых радиофармацевтических лекарственных препаратов (РФЛП) — один из главных трендов в ядерной медицине. В последние годы появилось около 10 новых изотопных препаратов, в частности, Lutathera (177Lu-DOTATATE), Lymphoseek (технеций (99mTc) тилманосепт), NetSpot (68Ga-DOTATATE) и др. Область радиофармацевтики привлекает большое внимание, в том числе из-за увеличения количества исследований методом позитронно-эмиссионной томографии (ПЭТ), возрастающих потребностей не только в традиционных радиоизотопах, таких как 11С, 13N, 15O, 18F, но и генераторных 68Ga и 82Rb, а также в связи с необходимостью поиска новых решений для улучшенной диагностики при сочетании ПЭТ и компьютерной томографии2.
В настоящее время в мире одобрены для использования 67 РФЛП (по международным непатентованным наименованиям) [1]. Согласно Государственному реестру лекарственных средств в Российской Федерации зарегистрировано 62 РФЛП, 47 из них диагностические на основе изотопов технеция [ 99mTс], йода ([ 131I], [123I]) и фтора [ 18F]3. Из 62 зарегистрированных РФЛП лишь 4 зарубежного производства, остальные — отечественные.
Объем производства РФЛП крайне мал по сравнению с другими лекарственными средствами (количество упаковок в серии составляет несколько единиц [2]), срок годности препаратов, в зависимости от периода полураспада соответствующих радионуклидов, составляет от нескольких минут до нескольких суток. В связи с этим осуществление фармацевтической разработки, проведение доклинических и клинических исследований радиофармацевтических лекарственных препаратов, а также государственная регистрация происходят в особом порядке4.
РФЛП могут классифицироваться по различным признакам, включая вид излучения, тип радионуклида или способ введения. Однако в рамках данной работы акцент сделан на классификации РФЛП по направлению их медицинского применения. Выделяют три основные группы: диагностические препараты, терапевтические препараты, препараты тераностики [3].
Диагностические РФЛП, предназначенные для визуализации физиологических и патологических процессов, содержат короткоживущие гамма-излучающие или позитрон-излучающие нуклиды, обладают минимальной радиотоксичностью, они должны иметь высокую специфичность и быстрый клиренс из организма. Терапевтические РФЛП содержат α- или β-излучающие нуклиды, должны специфично накапливаться в патологическом очаге, обеспечивать ограниченное облучение здоровых тканей и, как правило, требуют индивидуального дозиметрического подхода.
В последние годы все большее внимание уделяется РФЛП, которые находятся на стыке двух этих направлений — тераностике. РФЛП для радиотераностики представляют собой одну или пару молекул с одинаковым биологическим носителем, но разными радионуклидами, что позволяет использовать диагностическую визуализацию для отбора пациентов и планирования терапии, обеспечивая персонифицированный подход к лечению, а именно повышение эффективности лечения и снижение побочных эффектов [4][5].
В условиях столь динамичного развития отрасли крайне важно отслеживать происходящие изменения, особенно учитывая стремление российских разработчиков сохранить и укрепить позиции среди мировых лидеров отрасли. Чтобы своевременно реагировать на возникающие вызовы, соответствовать мировым трендам и корректировать собственную стратегию развития, необходим объективный и проверенный инструмент анализа. Одним из таких инструментов является патентный анализ: в патентных заявках разработчики раскрывают свои технологические решения, а сами охранные документы служат не только индикатором инновационной активности, но и механизмом ограничения конкурентов, предоставляя временную правовую монополию на разработки.
Цель работы — комплексный анализ патентной активности в радиофармацевтике для оценки ее современного состояния и выявления ключевых векторов технологического развития.
Задачи исследования:
1) определение состояния существующих исследований в области разработки и применения РФЛП через патентный анализ;
2) выявление ключевых исследователей и разработчиков;
3) определение перспективных направлений развития данной области.
МАТЕРИАЛЫ И МЕТОДЫ
Для достижения цели исследования использовались методы патентного поиска, патентного анализа, библиометрического анализа, методы сегментирования научно-технической информации.
Для формирования комплексного обзора тенденций по разработке РФЛП был проведен поиск патентных документов, раскрывающих структуры химических соединений, композиции, составы, способы получения, способы лечения, применение РФЛП для лечения и (или) диагностики заболеваний.
Патентный поиск реализован c использованием базы данных «Questel Orbit» (БД Orbit). Глубина патентного поиска составила 25 лет (с 01.01.2000 по 31.12.2024). Ограничения по юридическому статусу патентного документа или географии патентования не применялись.
Единицей исследования является патентное семейство (все патентные публикации, относящиеся к одному изобретению). Патентные семейства обладают несколькими полезными свойствами: исключают дублирование, устраняют языковые барьеры, указывают на географию изобретения, раскрывают технологические тренды.
Для отбора патентов были использованы индексы Международной патентной классификации (МПК): A61K 49/00; A61K 31/00; A61K 51/00; A61K 101/00; A61K 103/00; C07B 59/00. Для проведения патентного поиска помимо индексов МПК был сформирован перечень ключевых слов, которые использовались для составления поисковых запросов в базе данных Orbit c применением поисковых операторов системы. В качестве областей поиска ключевых слов были использованы следующие разделы патентного документа: название, реферат, описание и формула. В качестве ключевых слов были использованы общие термины, характерные для описания РФЛП.
Ключевые слова, используемые при формировании поискового запроса на английском языке: radiopharmaceuticals, radionuclide, radioisotope, radiotracer, diagnostic imaging, rаdionuсlide labeled therapy, radiotherapeutic agent, radiodiagostic agent, radioactive, single photon emission computed tomography, PET, SPECT, positron emission tomography, scintigraphy, scintigraphic imaging, brachytherapy, therapeutic, diffusing alpha-emitter radiation therapy, DaRT, PRRT, SIRT, selective internal radiation therapy, theragnostic, theranostic, diagnostic, radioembolisation, peptide-receptor radionuclide therapy, radioactive drug.
Ключевые слова, используемые при формировании поискового запроса на русском языке: РФП, РФЛП, радиофарм+, радиоактивн+, радионуклид, позитронно-эмиссионная томография, сцинтиграфия, однофотонная эмиссионная компьютерная томография, однофотонная эмиссионная компьютерная томография, ПЭТ, радионуклидная терапия, лучевая терапия, радиодиагностика, лучевая радионуклидная диагностика, клиническая радиология, радиофармацевтическая композиция, РФК, авторадиография, брахиотерапия, радиоизотопная терапия, радиоизотоп, радиоэмболизация.
Патентные документы, содержащие в формуле изобретения, как РФЛП и их применение, так и узлы диагностического оборудования и (или) способ наработки радиоизотопов, указание на радиофармацевтический предшественник, не были исключены из коллекции и приняты к рассмотрению в связи с наличием в них объектов исследования, указанных в независимых пунктах формулы.
Процедура очистки патентной коллекции включала исключение нерелевантных документов, не содержащих в формуле изобретение РФЛП или их применение, а также устранение дубликатов за счет анализа патентных семейств. Кроме того, верификация данных проводилась методом ручной выборочной проверки патентных документов, что обеспечило соответствие выборки целям и предмету исследования, а также повысило качество и достоверность полученной патентной базы.
В результате сформирована актуальная и валидная коллекция патентных данных, охватывающая исследования по радиофармацевтическим композициям, их применению в диагностике, терапии и тераностике, а также способам получения и доставки данных препаратов. Такая методология позволила комплексно рассмотреть глобальные тренды патентования в области радиофармацевтики.
В ходе проведения патентного поиска были определены основные объекты патентования:
- радиофармацевтические композиции, выраженные в структурных формулах химических соединений, составах, конъюгатных комплексах, включающие радионуклиды и применяемые в качестве диагностических, тераностических или терапевтических агентов;
- применение таких композиций для лечения заболеваний;
- применение таких композиций в диагностических методах и методах медицинской визуализации;
- способы доставки, способы получения указанных композиций.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
По результатам поиска всего выявлено 4988 патентных семейств за период 2000–2024 гг. Около 60% патентных семейств поддерживаются в силе, то есть включают действующие патенты или патентные заявки, по которым продолжается делопроизводство.
Около 16% патентных семейств коллекции принадлежат 10 компаниям-патентообладателям, что говорит о том, что в мире относительно невысокий уровень технологической монополизации. В рассматриваемой области присутствует достаточно много участников, конкурентная среда выглядит в целом сбалансированной, представленной и университетами, и научными организациями, и компаниями — представителями списка «Big Pharma» («Большая фарма»)5, а также малыми и средними коммерческими компаниями. Сбалансированность также отмечается с точки зрения принадлежности держателей технологий различным странам — держатели технологий распределены как в США, так и в Европе, и в Азии, при этом в основном относятся к технологически развитым странам. Общая динамика патентной активности представлена на рисунке 1: первые (приоритетные) заявки патентных семейств указывают на динамику появления новых исследований и разработок в области; выданные патенты указывают на коммерческий и продуктовый потенциал разработок; общая динамика патентных публикаций иллюстрирует стратегии патентной охраны заявителей и патентообладателей, в частности их интерес к распространению новых технологий по географическому признаку, а также использование методов комплексной правовой охраны разработок, указывающих на переход к более зрелой стадии коммерциализации технологий.
Рост числа новых разработок был плавным до 2018 г. и не превышал 200 новых патентных семейств в год. Начиная с 2018 г. темпы роста возникновения новых патентных семейств увеличились, и с 2020 по 2022 гг. произошел резкий рост числа приоритетных заявок, свидетельствующий об активизации исследований и разработок в рассматриваемой технологической области.
В первую очередь отмеченный рост можно связать с клиническими успехами и одобрением к применению таких РФЛП, как 177Lu-DOTATATE (Lutathera) и 177Lu-PSMA-617 (Pluvicto)6. Данные препараты позволили эффективно проводить терапию заболеваний, для которых ранее не существовало эффективных методов лечения, что вызвало волну интереса к разработке аналогичных средств, в том числе к поиску новых конъюгатов и методов доставки радионуклидов [6]. Также следует отметить, что одобрение Управления по контролю за качеством продуктов питания и лекарственных средств США (Food and Drug Administration, FDA) первого 68Ga, специфичного для предстательной железы мембранного антигена, — [ 68Ga] Ga-PSMA-11 повлияло на увеличение патентных заявок на PSMA-таргетированные лиганды и их синтез [7].
Начиная с 2022 г. количество новых патентных семейств снижается. В первую очередь это связано с особенностями публикации патентных документов. По общему правилу в соответствии с международными соглашениями7 публикация патентных документов происходит через 18 мес. после даты подачи патентной заявки. Это означает, что по состоянию на момент исследования полные данные по заявкам представлены на момент, когда не все заявки, поданные в 2023–2024 гг., опубликованы. Следует ожидать продолжающегося роста патентных публикаций 2023–2024 гг. накопительным итогом.
Продолжающееся в настоящее время наращивание массы патентных публикаций в мире, подкрепленное устойчивым ростом патентных заявок, говорит о том, что предметная область находится на пике интереса с точки зрения коммерциализации и выхода на новые рынки.
Анализ рассматриваемой патентной коллекции позволяет также представить распределение правовых статусов патентных семейств по годам (рис. 2) (распределение по годам действующих патентных семейств, недействующих патентных семейств (нет действующих патентов и нет патентных заявок, по которым ведется или может быть продолжено делопроизводство)), а также семейств, в которых есть только заявки, по которым ведется делопроизводство8.
Даже самые ранние годы приоритетов включают действующие патентные семейства, которые, как правило, являются корневыми для направлений предметной области. 2013 год был переломным, так как число действующих патентных семейств становится больше числа недействующих и далее поступательно растет, с каждым годом увеличивая долю новых семейств среди действующих.
Сопоставляя данные рисунков 1 и 2, можно предположить, что в 2018–2020 гг. произошел существенный технологический скачок, определяющий до настоящего времени состояние развития технологий в радиофармацевтике. При этом следует отметить, что в области не происходит резкого замещения технологий, ранние технологии по-прежнему актуальны. Период 20-летней ретроспективы следует рассматривать как с точки зрения потенциала коммерциализации, так и с точки зрения базы для развития будущих технологий. Можно также отметить, что в последние 5–7 лет в распределении правовых статусов присутствует существенная доля утративших силу патентных семейств, что говорит о том, что 15–20% разработок не переходят на продуктовые стадии разработок. Это обстоятельство следует учитывать при планировании финансирования ранних фаз разработок в предметной области.
На рисунке 3 патентная коллекция по радиофармацевтике рассмотрена с точки зрения распределения патентных семейств по странам наиболее раннего приоритета патентных семейств. Такое распределение говорит о происхождении новых разработок, так как заявители, как правило, подают первые патентные заявки в патентное ведомство, соответствующее стране их резиденции. Круг стран, в которых ведутся исследования и разработки и которые являются, по сути, пионерами радиофармацевтических технологий, достаточно ограничен. Приоритеты разработок для более чем 90% всей коллекции приходятся всего на 10 стран (США, КНР, Россия, Великобритания, Япония, Республика Корея, Австралия, Германия, Тайвань, Италия). При этом доминирующая роль у США и КНР, находящихся в состоянии технологической гонки в предметной области.
Для иллюстрации динамики исследований и разработок в области РФЛП по странам в таблице 1 представлена тепловая карта появления приоритетных заявок по стране происхождения. В последние годы самые высокие темпы роста исследовательской активности демонстрируют организации из КНР. Компании из США также наращивают темпы патентования, оставаясь при этом лидерами, с учетом многолетней постоянной активности в рассматриваемой области. Организации из европейских стран и России на протяжении последних 5–7 лет демонстрируют умеренный рост.
Другим важным индикатором локализации технологий радиофармацевтики является география стран патентной охраны (включает выданные патенты по странам), показывающая распространение технологий по миру и соответствующие рынки сбыта продукции (рис. 4). Помимо стран, ведущих исследования и разработки, к числу развитых рынков сбыта следует отнести Канаду, Мексику, Индию, Израиль, Бразилию. Всего с точки зрения патентной охраны отмечается более 40 стран с устойчивым присутствием запатентованных технологий, что необходимо учитывать российским разработчикам и производителям РФЛП при планировании территориальной экспансии разработок.
Особенности патентования в области РФЛП
При структурном анализе было определено, что большинство поданных патентных документов относятся к диагностическим РФЛП (43%), применяющимся для визуализации и выявления заболеваний. Патентные документы, относящиеся к терапии, составляют 23% от всех патентных документов, а к тераностике — 34%.
Начиная с 2019 г. рост патентования области в целом обеспечивался за счет новых решений в области тераностики (рис. 5). В первую очередь рост связан с появлением современных инновационных РФЛП, содержащих в своем составе радионуклиды с повышенной стабильностью и направляющие молекулы, что позволяет доставлять радионуклид непосредственно к опухолям с минимальными побочными эффектами. В таких случаях РФЛП позволяют одновременно диагностировать опухоль и проводить лечение в реальном времени. Примерами таких препаратов являются инновационные Lutathera (177Lu-DOTATATE) для лечения нейроэндокринных опухолей и Pluvicto (177Lu-PSMA-617) для лечения кастрационно-резистентного рака предстательной железы и их дополнительные диагностические визуализирующие агенты Netspot (Ga-68-DOTATATE) и Locametz ([ 68Ga]Ga-68-PSMA-11).
В то же время стоит отметить, что начиная с 2021 г. произошел рост в отношении терапевтических РФЛП. Этому способствовало в том числе прогнозируемое увеличение рынка радиофармацевтики до 16 млрд долларов США к 2030 г. при среднем ежегодном темпе роста 27%, что обусловило активизацию научно-исследовательских работ и сопутствующее усиление патентования в секторе терапевтических РФЛП9.
Таким образом, современные тренды патентования определяют решения в области тераностики и терапии. При этом диагностика сохраняет свои позиции, оставаясь в состоянии стабильного плато ежегодного прироста новых изобретений. США лидируют по всем трем сегментам, и только в диагностике США разделяет лидерство с КНР. Отмечаются уверенные позиции России в диагностике и терапии (табл. 2).
Лидером во всех рассматриваемых направлениях (рис. 6) является компания GE Healthcare. GE Healthcare, вышедшая из состава компании General Electric в качестве самостоятельной компании, за последние два года поглотила несколько профильных радиофармацевтических компаний10, таких как MACTIS SAS (январь 2023 г.) — французская компания, которая разрабатывает и производит системы интервенционной радиологии для применения в здравоохранении, MIM Software (январь 2024 г.) — компания из Огайо, которая предоставляет практические решения для визуализации в таких областях, как радиационная онкология, радиология для сектора здравоохранения, Nihon Medi Physics (декабрь 2024 г.) — ведущая радиофармацевтическая компания Японии. Благодаря поглощению последней GE Healthcare увеличила свой патентный портфель по решениям в области радиофармацевтики на 30%.
Необходимо отметить, что GE Healthcare является держателем регистрационных удостоверений на лекарственные препараты в сфере радиофармацевтики в России, что может привести к риску усиления влияния иностранных организаций на российский рынок РФЛП.
Особое внимание стоит обратить на состав патентного портфеля компании Actinium Pharmaceuticals, которая занимает лидирующую позицию в самой трендовой области патентования — терапии. Actinium Pharmaceuticals — это биофармацевтическая компания, специализирующаяся на разработке таргетной радиотерапии для лечения онкологических заболеваний, особенно у пациентов, не ответивших на существующие методы терапии. Основные направления деятельности компании включают разработку препаратов для подготовки пациентов к трансплантации костного мозга и улучшения исходов клеточной и генной терапии. Компания активно использует изотоп 225Ac, обладающий высокой способностью разрушать ДНК раковых клеток за счет альфа-излучения. В свою очередь, в сегменте диагностики РФЛП у компании нет охранных документов.
Отдельное внимание стоит уделить патентному портфелю компании Novartis, которая является правообладателем на такие РФЛП, как Lutathera и Pluvicto.
Патенты на препарат Lutathera, перечисленные в «Оранжевой книге»11 FDA (US10596276, US10596278, US11904027, US12144873, US12151003, US12161732, US12168063), принадлежат Advanced Accelerator Applications (дочерней компании Novartis). Все перечисленные патенты связаны с изобретениями в области стабильных, концентрированных растворов радионуклидных комплексов, которые используются в составе Lutathera. В объем правовой охраны указанных охранных документов входят составы радиофармацевтических растворов, способы их стабилизации, способы производства, а также способы терапевтического применения. Кроме того, известна судебная практика по защите патентов Lutathera, включая споры, например, с Evergreen Theragnostics, Inc., которые были разрешены в пользу правообладателя12. В совокупности данные патенты формируют комплексную правовую охрану против прямого копирования основных технологических решений в составе Lutathera, что защищает позиции Advanced Accelerator Applications на рынке терапевтических РФЛП для лечения нейроэндокринных опухолей.
Патенты на препарат Pluvicto, перечисленные в «Оранжевой книге»13 FDA (US10398791, US10406240, US11318121, US11951190, US12208102), принадлежат Novartis и ее дочерним компаниям, в частности Purdue Research Foundation. Все указанные патенты связаны с изобретениями, которые обеспечивают охрану структуры химического соединения — ингибитора PSMA, конъюгатов, способов стабилизации, а также способов терапевтического применения препарата Pluvicto для лечения PSMA-позитивного метастатического кастрационно-резистентного рака простаты. В совокупности данные патенты формируют комплексную правовую охрану ключевых технологических аспектов создания препарата. Таким образом, компания сохраняет сильную патентную охрану Pluvicto, препятствуя прямому копированию и обеспечивая сильные позиции на рынке РФЛП для терапии рака простаты.
Из числа российских организаций в списке лидеров (рис. 6) достаточно высокую позицию занимает Томский научный исследовательский медицинский центр Российской академии наук (Томский НИМЦ). Томский НИМЦ занимается разработкой диагностических препаратов по двум ключевым направлениям: онкология и хирургия. В частности, в 2024 г. была запатентована молекула, схожая по принципу действия с Lutathera и Pluvicto, для лечения рака молочной железы, которая может стать третьей в мире уникальной молекулой для направленной радиотераностики в онкологии [8]. Уже более двадцати лет наблюдается активность получения охранных документов в данных нозологиях, но в последние годы Томский НИМЦ набирает темп формирования патентного портфеля организации и, соответственно, закладывает прочные основы в развитии РФЛП на территории России.
В ходе исследования дополнительно также были проанализированы формулы изобретений. Далее рассмотрены наиболее выделяющиеся примеры формулирования объема патентной охраны.
Мемориальный онкологический центр имени Слоуна–Кеттеринга (Memorial Sloan Kettering Cancer Center (MSKCC)) обладает одной из самых обширных патентных коллекций по разработке средств в сфере тераностики, компания сосредоточена на патентовании биологических и клеточных терапий, вирусных векторов, а также соединений, комплексов, композиций и методов для диагностики и терапии злокачественных новообразований и других заболеваний. Рассматриваемый центр демонстрирует комплексный подход к формированию стратегии получения правовой охраны разработок. Кроме того, в формулах изобретений охраняется продукт для радиофармацевтической терапии, меченный изотопом, который выбран из группы, и представлен перечень радионуклидов, а также экспериментальные данные, подтверждающие реализацию назначения изобретения.
Из российских организаций для анализа был выбран патентный портфель Томского политехнического университета, который специализируется на разработке комплексов для радионуклидной диагностики злокачественных новообразований, а также средств в области тераностики по получению комплекса с радионуклидной меткой для диагностики и терапии рака предстательной железы, а также рака молочной железы. В формулах изобретений содержится указание на один конкретный радионуклид, который применяется при изготовлении РФЛП.
Таким образом, при сравнении стратегий патентования зарубежной и российской организаций было выявлено, что зарубежные компании составляют формулу изобретения широко, в частности включают описание состава, способа получения или применения РФЛП с использованием максимально общих характеристик (например, класса радионуклидов, группы молекулярных носителей или методов введения), что позволяет патенту охватывать множество вариантов подобных препаратов, охраняя не только конкретную молекулу, но и ее аналоги, и затрудняя разработку конкурирующих средств с обходом патентных прав. В то же время российские организации получают точечные патенты, которые охраняют определенные химические соединения, методы синтеза РФЛП, конкретные фармацевтические композиции или уникальные способы введения радиоактивных изотопов, что обеспечивает охрану именно этих отдельных аспектов без охвата более широкого класса веществ.
Соответственно, с целью усиления правовой охраны разработок российским организациям необходимо включать в объем притязаний диапазоны значений (например, доз, компонентов), группы радионуклидов, экспериментальные данные, примеры, подтверждающие достижение указанного технического результата для укрепления правовой охраны и дальнейшей коммерциализации разработки.
Помимо патентной активности важно также учитывать практические разработки и участие российских организаций в создании РФЛП. Среди российских разработчиков в области ядерной медицины стоит отметить Госкорпорацию «Росатом» (ГК «Росатом»), которая, будучи одним из ключевых игроков на мировом рынке радиоизотопов промышленного и медицинского назначения, разрабатывает линейку РФЛП (более 10 препаратов). Область применения — таргетная терапия рака простаты, диагностика и терапия трехнегативного рака молочной железы и др.14
Среди российских разработчиков можно также выделить ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, у которого в настоящий момент три РФЛП (артрорен-МРНЦ с 188Re для лечения хронических воспалительных заболеваний суставов, сопровождающихся синовитом, — радиосиновэктомии; гепаторен-МРНЦ с 188Re для лечения неоперабельных опухолей печени; 225Ас-DOTA-PSMA для лечения пациентов с метастатическим раком печени, которым не помогла терапия РФЛП Лютапрост-МРНЦ) уже находятся на стадии клинических исследований. В разработке находится еще один РФЛП 225Ас-DOTATOC для лечения пациентов с нейроэндокринными злокачественными новообразованиями в случае неэффективности терапии РФЛП 177Lu-DOTATOC [9].
В портфеле ФГБУ «РНЦРХТ им. ак. А.М. Гранова» Минздрава России более 10 разработок РФПЛ, находящихся на разных этапах исследования, в том числе на основе радионуклидов металлов и однодоменных антител (наноантител) к PD-L1 и HER-215.
Разработкой РФЛП занимаются такие передовые научные институты, как федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр онкологии имени Н.Н. Блохина» Министерства здравоохранения Российской Федерации, федеральное государственное бюджетное учреждение «Государственный научный центр Российской Федерации — Федеральный медицинский биофизический центр имени А.И. Бурназяна» Федерального медико-биологического агентства, федеральное государственное бюджетное учреждение «Национальный исследовательский центр «Курчатовский институт» и др.16
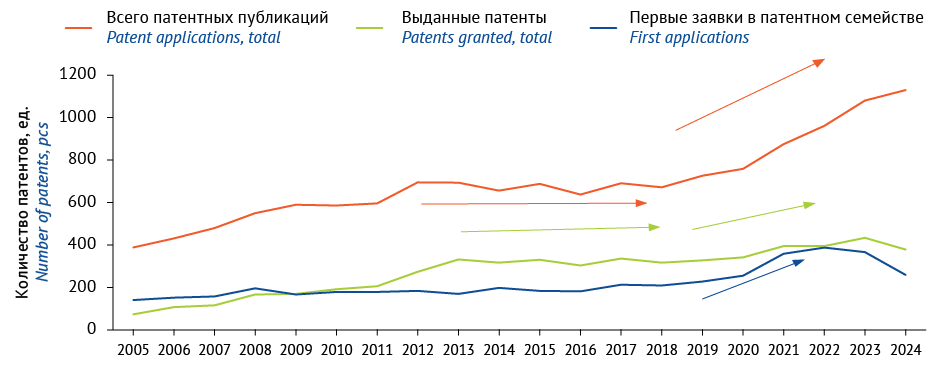
Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 1. Динамика патентной активности в области радиофармацевтических лекарственных препаратов
Fig. 1. Dynamics of patent activity in the field of radiopharmaceuticals
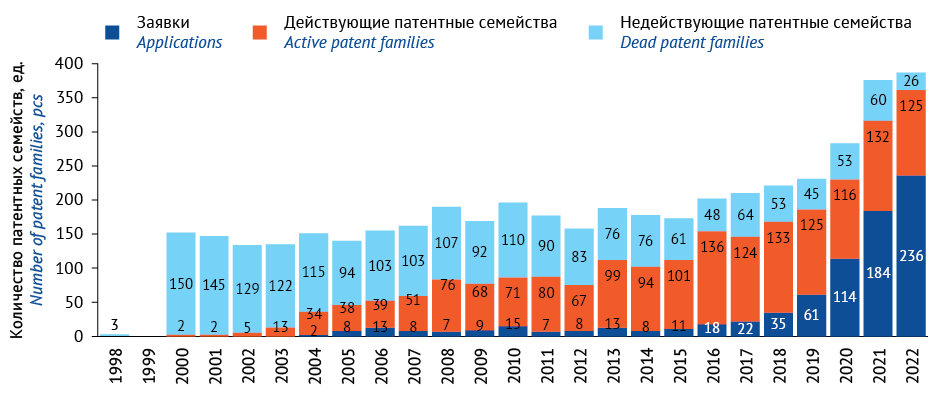
Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 2. Распределение правовых статусов патентных семейств в области радиофармацевтических лекарственных препаратов по годам наиболее ранних приоритетов патентных семейств
Fig. 2. Yearly distribution of legal status of patent families in the field of radiopharmaceuticals (the earliest priorities of patent families)

Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 3. Распределение патентных семейств в области радиофармацевтических лекарственных препаратов по странам наиболее раннего приоритета
Fig. 3. Distribution of patent families of radiopharmaceuticals by countries of the earliest priority
Таблица 1. Тепловая карта распределения приоритетных патентных заявок в области радиофармацевтических лекарственных препаратов по странам происхождения
Table 1. Heatmap of priority patent applications of radiopharmaceuticals distributed by country of origin
|
Патентные ведомства по странам Patent offices by country |
Годы Years |
|||||||||||||||||||
|
2005 |
2006 |
2007 |
2008 |
2009 |
2010 |
2011 |
2012 |
2013 |
2014 |
2015 |
2016 |
2017 |
2018 |
2019 |
2020 |
2021 |
2022 |
2023 |
2024 |
|
|
США USA |
83 |
80 |
92 |
87 |
73 |
60 |
83 |
83 |
68 |
96 |
79 |
67 |
73 |
77 |
72 |
70 |
116 |
108 |
102 |
81 |
|
Китай China |
4 |
6 |
7 |
39 |
31 |
25 |
22 |
23 |
27 |
31 |
30 |
40 |
42 |
46 |
63 |
103 |
134 |
167 |
171 |
150 |
|
Европейское патентное ведомство European Patent Office |
11 |
14 |
18 |
17 |
9 |
17 |
15 |
16 |
9 |
8 |
13 |
16 |
20 |
15 |
19 |
23 |
28 |
31 |
28 |
10 |
|
Россия Russia |
5 |
6 |
10 |
11 |
4 |
3 |
9 |
6 |
14 |
12 |
7 |
14 |
18 |
19 |
19 |
11 |
17 |
30 |
19 |
4 |
|
Великобритания Great Britain |
18 |
16 |
4 |
7 |
16 |
12 |
10 |
9 |
12 |
6 |
8 |
8 |
7 |
4 |
2 |
5 |
6 |
6 |
0 |
0 |
|
Япония Japan |
4 |
6 |
9 |
6 |
5 |
15 |
4 |
9 |
9 |
14 |
8 |
6 |
12 |
13 |
10 |
6 |
2 |
9 |
10 |
1 |
|
Республика Корея Republic of Korea |
1 |
5 |
3 |
7 |
4 |
7 |
8 |
7 |
12 |
9 |
11 |
11 |
9 |
13 |
14 |
11 |
8 |
10 |
2 |
0 |
|
Австралия Australia |
0 |
4 |
1 |
2 |
4 |
0 |
4 |
6 |
5 |
1 |
4 |
2 |
4 |
1 |
4 |
6 |
6 |
5 |
9 |
5 |
|
Германия Germany |
3 |
2 |
1 |
5 |
3 |
14 |
4 |
5 |
2 |
1 |
0 |
0 |
3 |
3 |
3 |
1 |
4 |
1 |
2 |
0 |
|
Тайвань Taiwan |
1 |
0 |
3 |
2 |
6 |
8 |
5 |
3 |
4 |
7 |
9 |
3 |
4 |
5 |
4 |
4 |
3 |
4 |
1 |
0 |
|
Италия Italy |
0 |
3 |
1 |
3 |
1 |
1 |
2 |
0 |
3 |
1 |
0 |
3 |
1 |
2 |
3 |
3 |
3 |
1 |
1 |
0 |
|
Франция France |
1 |
2 |
4 |
2 |
2 |
3 |
0 |
5 |
3 |
1 |
0 |
1 |
3 |
0 |
1 |
1 |
0 |
0 |
0 |
0 |
|
Индия India |
1 |
0 |
1 |
2 |
0 |
1 |
1 |
1 |
0 |
1 |
4 |
1 |
1 |
2 |
2 |
0 |
3 |
2 |
4 |
0 |
Таблица составлена авторами / The table is prepared by the authors
Примечание. Цветовая заливка в таблице обозначает интенсивность появления новых технологий в сфере РФЛП по стране происхождения разработки.
Note. The colour in the table indicates the rate of emergence of new radiopharmaceutical technologies by the country of origin.
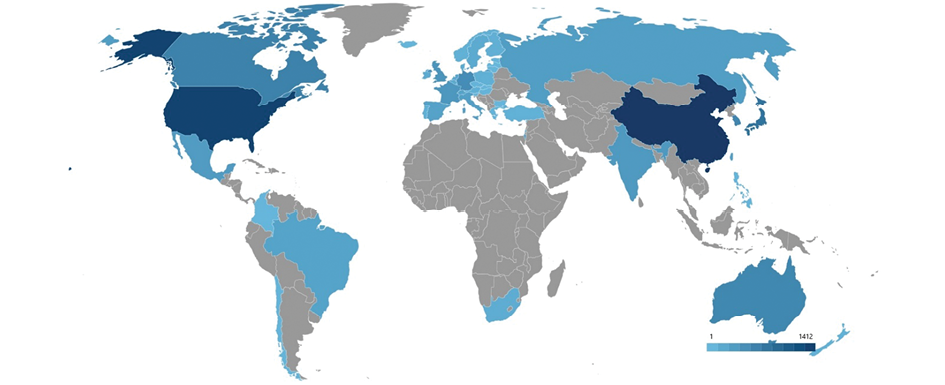
Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 4. География патентования по странам с выданными патентами в области радиофармацевтических лекарственных препаратов
Fig. 4. Geographical distribution of patenting by countries, with patents granted to radiopharmaceuticals

Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 5. Динамика патентной активности в области применения радиофармацевтических лекарственных препаратов по годам
Fig. 5. Dynamics of patent activity for radiopharmaceuticals by year
Таблица 2. Динамика исследований и разработок в области применения радиофармацевтических лекарственных препаратов по странам в 2005–2024 гг.
Table 2. Dynamics of research and development of radiopharmaceuticals by country, 2005–2024
|
Патентные ведомства по странам Patent offices by country |
Область применения Scope of application |
||
|
Диагностика Diagnostics |
Тераностика Theranostics |
Терапия Treatment |
|
|
США USA |
665 |
760 |
507 |
|
Китай China |
613 |
332 |
221 |
|
Европейское патентное ведомство European Patent Office |
111 |
165 |
91 |
|
Россия Russia |
183 |
25 |
51 |
|
Великобритания Great Britain |
86 |
68 |
54 |
|
Япония Japan |
104 |
47 |
31 |
|
Республика Корея Republic of Korea |
90 |
46 |
26 |
|
Австралия Australia |
23 |
27 |
30 |
|
Германия Germany |
39 |
28 |
13 |
|
Тайвань Taiwan |
35 |
24 |
16 |
|
Италия Italy |
10 |
21 |
9 |
|
Франция France |
11 |
12 |
10 |
|
Индия India |
12 |
10 |
3 |
|
Дания Denmark |
9 |
10 |
5 |
|
Бразилия Brazil |
10 |
5 |
3 |
|
Норвегия Norway |
7 |
2 |
8 |
|
Швеция Sweden |
4 |
10 |
3 |
Таблица составлена авторами / The table is prepared by the authors
Примечание. Цветовая заливка в таблице обозначает интенсивность появления новых технологий в сфере РФЛП по стране происхождения разработки.
Note. The colour in the table indicates the rate of emergence of new radiopharmaceutical technologies based on the country of origin.

Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 6. Рейтинг организаций-патентообладателей в области радиофармацевтики с распределением действующих патентных семейств по основным трем направлениям применения
Fig. 6. Ranking of organisations holding radiopharmaceutical patent, with distribution of active patent families by the three main applications
ЗАКЛЮЧЕНИЕ
Одним из ключевых направлений развития ядерной медицины в мире является разработка и внедрение в практику новых радиофармацевтических препаратов, что коррелирует с международными прогнозами рынка РФЛП.
Проведенный патентный анализ демонстрирует тенденцию перехода от диагностических к тераностическим технологиям: современные разработки (например, универсальные пептидные платформы) интегрируют диагностику и терапию в единые решения для рака простаты, нейроэндокринных опухолей. Технологическое лидерство сосредоточено преимущественно в США, КНР и странах Европейского союза, обладающих развитой научно-технической инфраструктурой и высоким коммерческим потенциалом.
Выявлено несоответствие существующего научного задела российских исследовательских центров и патентной активности в сегменте тераностических РФЛП. Для повышения конкурентоспособности российских решений на международной арене необходимо не только ускорить темпы фундаментальных и прикладных исследований, но и оптимизировать патентные стратегии, что позволит более надежно охранять инновационные технологии от обхода и формировать устойчивое конкурентное преимущество. Внедрение таких комплексных подходов будет способствовать эффективной коммерциализации отечественных разработок и станет стимулом к привлечению инвестиций, развитию международного сотрудничества и расширению присутствия российских радиофармацевтических препаратов на мировом рынке.
1 Паспорт национального проекта «Продолжительная и активная жизнь».
Национальный проект «Продолжительная и активная жизнь: новые задачи здравоохранения до 2030 года».
2 BRICS Overview of best practices on nuclear medicine, 2024.
3 Государственный реестр лекарственных средств.
4 Решение Совета ЕЭК от 03.11.2016 № 78 «О Правилах регистрации и экспертизы лекарственных средств для медицинского применения».
5 The Pharma 1000: Top global pharmaceutical companies.
6 Fattorini F. Radiopharmaceutical deals drive sector growth despite supply crisis. Pharmaceutical Technology. 2025.
7 Договор о патентной кооперации (Patent Cooperation Treaty, PCT): международный договор, подписанный в г. Вашингтон 19.06.1970.
8 Такие семейства, как правило, относятся к «молодым» патентным семействам, характеризующим ранние стадии новых разработок.
9 The state of radiopharmaceutical therapy. Cardinal Health; 2021.
10 List of GE Healthcare’s Acquisitions.
11 Orange Book: Approved drug products with therapeutic equivalence evaluations.
12 PGR2021-00002 — Evergreen Theragnostics Inc v. Advanced Accelerator Applications SA.
13 Там же.
14 Мирный атом на страже здоровья. Как «Росатом» внедряет в России лечение радиофармпрепаратами. Росатом Наука. 2024.
Росатом намерен увеличить с 2025 года число выпускаемых радиофармпрепаратов с 11 до 25. ТАСС. 2023.
15 Государственное задание ФГБУ «РНЦРХТ им. ак. А.М. Гранова», 2022–2024.
16 ЕГИСУ НИОКТР. Домен «Наука и инновации».
Список литературы
1. Zhang S, Wang X, Gao X, et al. Radiopharmaceuticals and their applications in medicine. Signal Transduct Target Ther. 2025;10:1. https://doi.org/10.1038/s41392-024-02041-6
2. Кодина ГЕ, Малышева АО. Основные проблемы обеспечения качества радиофармацевтических лекарственных препаратов. Ведомости Научного центра экспертизы средств медицинского применения. 2019;9(4):216–30. https://doi.org/10.30895/1991-2919-2019-9-4-216-230
3. Ковальчук МВ, Деев СМ, Сергунова КА. Таргетная ядерная медицина. Достижения, проблемы и перспективы. Российские нанотехнологии. 2023;18(4):436–55. https://doi.org/10.56304/S1992722323040088 https://doi.org/10.1134/S2635167623700416
4. Filippi L, Chiaravalloti A, Schillaci O, et al. Theranostic approaches in nuclear medicine: Current status and future prospects. Expert Rev Med Devices. 2020;17(4):331–43. https://doi.org/10.1080/17434440.2020.1741348
5. Burkett BJ, Bartlett DJ, McGarrah PW, et al. A review of theranostics: Perspectives on emerging approaches and clinical advancements. Radiol Imaging Cancer. 2023;5(4):e220157. https://doi.org/10.1148/rycan.220157
6. Bodei L, Herrmann K, Schöder H, et al. Radiotheranostics in oncology: Current challenges and emerging opportunities. Nat Rev Clin Oncol. 2022;19(8):534–50. https://doi.org/10.1038/s41571-022-00652-y
7. Ute H, Eder M. [68Ga] Ga-PSMA-11: The first FDA-approved 68Ga-radiopharmaceutical for PET imaging of prostate cancer. Pharmaceuticals (Basel). 2021;14(8):713. https://doi.org/10.3390/ph14080713
8. Шеремет Н. В поисках уникальной молекулы. Территория интеллекта. 2025;(1):22–3.
9. Каприн АД. У радиофармпрепаратов в отечественной медицинской практике большое будущее. Ведомости Научного центра экспертизы средств медицинского применения. Регуляторные исследования и экспертиза лекарственных средств. 2022;12(4):359–61. https://doi.org/10.30895/1991-2919-2022-12-4-359-361
Об авторах
М. Ю. АникееваРоссия
Аникеева Марина Юрьевна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Ю. Д. Александров
Россия
Александров Юрий Дмитриевич.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Ю. А. Горбунова
Россия
Горбунова Юлия Александровна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Н. В. Попов
Россия
Попов Николай Васильевич.
Петровский б-р, д. 8, стр. 2, Москва, 127051
А. С. Кошевенко
Россия
Кошевенко Анастасия Сергеевна - канд. фарм. наук.
Петровский б-р, д. 8, стр. 2, Москва, 127051
В. В. Иващенко
Россия
Иващенко Валентина Владиславовна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Д. С. Иванова
Россия
Иванова Дарья Сергеевна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Е. Д. Николаева
Россия
Николаева Елена Дмитриевна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
А. В. Степанова
Россия
Степанова Александра Владимировна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Д. И. Федорова
Россия
Федорова Дарья Ильинична.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Дополнительные файлы
Рецензия
Для цитирования:
Аникеева М.Ю., Александров Ю.Д., Горбунова Ю.А., Попов Н.В., Кошевенко А.С., Иващенко В.В., Иванова Д.С., Николаева Е.Д., Степанова А.В., Федорова Д.И. Анализ глобальных трендов патентования в радиофармацевтике: диагностика, терапия и тераностика. Регуляторные исследования и экспертиза лекарственных средств. 2025;15(4):377-390. https://doi.org/10.30895/1991-2919-2025-15-4-377-390
For citation:
Anikeeva M.Yu., Aleksandrov Yu.D., Gorbunova Yu.A., Popov N.V., Koshevenko A.S., Ivashchenko V.V., Ivanova D.S., Nikolaeva E.D., Stepanova A.V., Fedorova D.I. Analysis of Global Patenting Trends in Radiopharmaceutical Industry: Diagnostics, Therapy, and Theranostics. Regulatory Research and Medicine Evaluation. 2025;15(4):377-390. (In Russ.) https://doi.org/10.30895/1991-2919-2025-15-4-377-390
JATS XML



































