Перейти к:
Технология получения и оценка качества микрокапсул сухого экстракта травы зюзника европейского (Lycopus europaeus L.)
https://doi.org/10.30895/1991-2919-2023-575
Резюме
АКТУАЛЬНОСТЬ. Гигроскопичность и низкая сыпучесть субстанции являются одной из проблем при производстве лекарственных препаратов на основе растительных экстрактов. Микрокапсулирование сухих экстрактов позволяет снизить их гигроскопичность, улучшить характеристики сыпучести и расширить область применения таких субстанций. Сравнительный анализ качества полученных микрочастиц в зависимости от выбранного метода микрокапсулирования необходим для последующей разработки лекарственных препаратов.
ЦЕЛЬ. Апробация разработанной ранее технологии получения микрокапсул и оценка качества микрочастиц сухого экстракта травы зюзника европейского.
МАТЕРИАЛЫ И МЕТОДЫ. Объектом исследования являлся сухой экстракт травы зюзника европейского, обладающий тиреостатическим действием. Микрокапсулирование проводилось методом диспергирования. Для формирования оболочек микрокапсул использован пленкообразователь — желатин марки П-11. Оценка характеристик полученных микрокапсул выполнена в соответствии с фармакопейными показателями качества: размер частиц, влажность, сыпучесть. Качественный и количественный анализ сухого экстракта травы зюзника европейского проводились методами тонкослойной хроматографии и спектрофотометрии.
РЕЗУЛЬТАТЫ. Подобраны оптимальные соотношения сухого экстракта, вспомогательных веществ и способа их введения при микрокапсулировании. Полученные микрокапсулы представляют собой однородные частицы размером 50–300 мкм с влажностью 3,21±0,12% и хорошей сыпучестью. Эффективность инкапсулирования при использовании метода диспергирования достигает 95,0±1,3%. Микрокапсулированные частицы экстракта в отличие от сухого экстракта обладают сферической формой, гладкой поверхностью и улучшенными технологическими показателями.
ВЫВОДЫ. Разработана технология микрокапсулирования сухого экстракта травы зюзника европейского. Результаты проведенных исследований подтвердили эффективность применения метода микрокапсулирования для снижения гигроскопичности сухого экстракта травы зюзника европейского и повышения его стабильности в процессе хранения, что позволит оптимизировать дальнейшую разработку лекарственных форм.
Ключевые слова
Для цитирования:
Семкина О.А., Белошапкина О.М. Технология получения и оценка качества микрокапсул сухого экстракта травы зюзника европейского (Lycopus europaeus L.). Ведомости Научного центра экспертизы средств медицинского применения. Регуляторные исследования и экспертиза лекарственных средств. 2024;14(1):72-80. https://doi.org/10.30895/1991-2919-2023-575
For citation:
Semkina O.A., Beloshapkina O.M. Production Technology and Quality Assessment of Microcapsules of Lycopus europaeus L. Herb Dry Extract. Bulletin of the Scientific Centre for Expert Evaluation of Medicinal Products. Regulatory Research and Medicine Evaluation. 2024;14(1):72-80. (In Russ.) https://doi.org/10.30895/1991-2919-2023-575
Введение
В условиях повышенного интереса к отечественному лекарственному растительному сырью1 и лекарственным препаратам растительного происхождения актуальными являются поиск и разработка методов производства, способствующих сохранению физико-химических и технологических свойств субстанций, в том числе сухих экстрактов. Сухие экстракты растительного происхождения характеризуются широким спектром фармакологической активности, хорошей переносимостью и низкой вероятностью возникновения побочных эффектов [1].
В Центре химии и фармацевтической технологии ФГБНУ ВИЛАР получен и стандартизован сухой экстракт травы зюзника европейского (Lycopus europaeus L.). Биологически активные вещества (розмариновая, кофейная, литоспермовая кислоты, инозид, лютеолин, эпигенин и др.), содержащиеся в экстракте зюзника европейского, оказывают выраженное тиреостатическое действие. По данным литературы, при введении в желудок лабораторных животных экстракт зюзника европейского оказывает седативный эффект и дозозависимое гипотиреоидное действие, связанное в основном с присутствием в экстракте розмариновой кислоты [2, 3].
Определение токсикологической характеристики экстракта, проведенное на мышах линии BALB/c и крысах Wistar обоего пола, показало, что фармацевтическая субстанция относится к классу малотоксичных веществ в соответствии с классификацией веществ по ГОСТ 12.1.007-762 [4].
Одной из проблем производства лекарственных препаратов на основе растительных экстрактов является гигроскопичность и низкая сыпучесть субстанции. Микрокапсулирование сухих экстрактов позволяет снизить гигроскопичность, улучшить характеристики сыпучести и расширить область применения полученных субстанций.
Существует более десяти методов микрокапсулирования, применяющихся для получения микрочастиц субстанций растительного происхождения: диспергирование, ионное гелеобразование, коацервация, распылительная сушка и др. [5, 6]. Для получения микрокапсул могут быть использованы не только отдельные методы, но и их комбинации, например последовательное применение методов диспергирования и распылительной сушки или метода коацервации совместно с лиофильной сушкой [7, 8].
Цель работы — апробация разработанной ранее технологии получения микрокапсул и оценка показателей качества микрочастиц сухого экстракта травы зюзника европейского.
Задачами исследования были получение микрокапсулированной формы экстракта травы зюзника европейского и оценка качества полученных частиц по показателям: влажность, подлинность, размер частиц, сыпучесть, угол естественного откоса, насыпная плотность.
Материалы и методы
Сухой экстракт травы зюзника европейского — аморфный порошок от светло-коричневого до зеленовато-коричневого цвета, специфического запаха. Для сухого экстракта характерна гигроскопичность и низкая сыпучесть. Сухой экстракт представлен частицами различной формы и размера, а именно: пластинами, параллелепипедами, овалами с неровными краями и шероховатой поверхностью. Размеры таких частиц варьируют от 10 до 100 мкм. Количественное содержание суммы фенольных соединений в пересчете на розмариновую кислоту в сухом экстракте составляет 7,2±0,4%. Сухой экстракт травы зюзника европейского растворим в воде очищенной, спирте этиловом 40%, частично растворим в маслах [9].
Вспомогательные вещества и растворители: желатин пищевой марки П-11 (ООО ТД «ХИММЕД»), глицерин (ч.д.а., ООО «АЛЬДОСА», кат. № 01.0.0.0208.02), алюминий хлористый 6-водный (квалификации BP/USP, ООО «АЛЬДОСА», кат. № 01.0.8.0007.07), кальций хлористый безводный (ч., ООО «АЛЬДОСА», кат. № 01.0.0.0451.07), этилацетат (х.ч., ООО «АЛЬДОСА», кат. № 01.0.3.0610.02), уксусная кислота ледяная (х.ч., ООО «АЛЬДОСА», кат. № 01.1.8.0620.02), масло вазелиновое (ФС.2.2.0004.15), масло терпентинное эфирное очищенное (ЛСР-002305/07, ФС.3.4.0014.18), вода очищенная (ФС 2.2.0020.18), спирт этиловый 96% (ФС 2.1.0036.15).
При получении микрокапсул использовали верхнеприводную мешалку RW 20 digital (IKA), вакуумный сушильный шкаф СНВС-25/3,5М (ООО «Тула-Терм»). Для определения потери в массе при высушивании объектов использовали анализатор влажности ML-50 (AND)3. Определение сыпучести проводили по скорости истечения из воронки с диаметром 10 мм4. Определение визуальных характеристик частиц проводили с использованием микроскопа цифрового МИКМЕД LCD 1000Х 2.0L (АО «ЛОМО»). Распределение частиц по размеру оценивали с использованием лазерного анализатора размера частиц Bettersizer SD (Bettersize)5. Количественное определение суммы фенольных соединений осуществляли на спектрофотометре Cary 100 Scan (Varian). Качественный анализ проводили методом тонкослойной хроматографии, пластинки Polyamide 11 F254 (Merck, кат. № 5557) размером 20×20 см в системе растворителей: этилацетат — концентрированная уксусная кислота — вода в объемном соотношении 5:1:1. В качестве образца сравнения использовали розмариновую кислоту (96%, Sigma-Aldrich, кат. № 536954).
При обработке полученных в ходе экспериментов результатов применяли метод вариационно-статистического анализа с оценкой значимости различий по критерию Стьюдента6.
Результаты и обсуждение
Для микрокапсулирования сухого экстракта травы зюзника европейского был выбран метод диспергирования. Выбор проведен с учетом физико-химических свойств субстанции, доступности способа получения микрокапсул, простоты аппаратного оформления и высокой производительности метода. Технологический процесс по методу диспергирования предполагает несколько этапов. На первом этапе получают раствор, содержащий пленкообразователь и активную действующую субстанцию (дисперсная фаза). На втором этапе при добавлении гидрофобной жидкости (дисперсионная среда — вазелиновое масло) образуются мягкие микрочастицы. На третьем этапе частицам придается упругость — при изменении температурного режима (охлаждение системы) затвердевает пленкообразующий материал.
Наиболее сложным является этап получения дисперсионной системы, для проведения которого важен выбор температурного режима, соотношения фазы и среды, скорости оборотов мешалки. Выбор условий для осуществления инкапсулирования на следующем этапе индивидуален и зависит не только от физико-химических свойств сухого экстракта и вспомогательных веществ, но и от используемых растворителей, а также ожидаемых формы и размера частиц, получаемых в результате инкапсулирования [10].
Для получения микрокапсул методом диспергирования в качестве пленкообразователя выбран желатин. Оптимальная концентрация желатина для предложенной технологии составляет 35–50% и зависит от формы выпуска желатина (порошок, гранулы, пластины), марки желатина и силы (прочности) геля желатина, которая определяется по методу Блюма7 и находится в пределах от 180 до 220 единиц. Если сила (прочность) геля используемого желатина менее 180 единиц, то сформированные микрочастицы могут слипаться на стадии охлаждения, что не позволит получить частицы размером менее 500 мкм. Если сила (прочность) геля используемого желатина выше 220 единиц, то процесс диспергирования осложнен неспособностью раствора к диспергированию при необходимой для получения микрочастиц температуре. Таким образом, для получения микрокапсул экстракта зюзника европейского был выбран желатин марки П-11.
В ходе эксперимента был разработан способ введения в липофильную среду сухого экстракта травы зюзника европейского — с предварительным растворением экстракта в растворе пленкообразователя — желатина. Полученную систему, содержащую экстракт и вспомогательные вещества, диспергировали с использованием мешалки (600 rpm, 50 °С) в присутствии масла вазелинового с последующим охлаждением системы до 0 °С. После охлаждения полученные частицы освобождали от дисперсионной среды и высушивали при температуре 35 °С в вакуумном сушильном шкафу. Технологическая схема получения микрокапсул представлена на рисунке 1.
Оценку качества полученных микрокапсул проводили по следующим показателям8: размер частиц, форма частиц, влажность, качественный анализ, угол естественного откоса, сыпучесть, насыпная плотность. Полученные результаты представлены в таблице 1.
Эффективность инкапсулирования (Эи, %) определяли на основании результатов спектрофотометрического анализа суммы фенольных соединений в пересчете на розмариновую кислоту и рассчитывали по формуле:
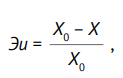 (1)
(1)
где Х0 — количество введенного в систему экстракта, Х — потери.
Методом диспергирования были получены микрочастицы диаметром 50–300 мкм, сферической формы с гладкой поверхностью (рис. 2). Рассчитанная по формуле (1) эффективность инкапсулирования составила 95,0±1,3% при влажности микрочастиц — 3,21±0,12%. Для исследования качественного состава полученных микрокапсул на линию старта хроматографической пластинки наносили 40 мкл спиртового извлечения сухого экстракта травы зюзника европейского 1%, 5 мкл спиртового раствора розмариновой кислоты 0,1% и 40 мкл спиртового извлечения микрокапсул сухого экстракта травы зюзника европейского 3%. На хроматограмме испытуемого раствора в ультрафиолетовом свете наблюдали светло-голубую зону адсорбции с Rf около 0,33, соответствующую аналогичной зоне адсорбции раствора розмариновой кислоты (рис. 3).
На рисунке 4 представлены интегральные кривые, отображающие распределение частиц экстракта по размерам. Средний размер частиц в образце сухого экстракта (D50) в соответствии с результатами проведенного исследования составил 65,1 мкм, для микрокапсулированной формы сухого экстракта D50 = 140,7 мкм. Полученные данные подтверждают, что для микрокапсулированной формы сухого экстракта характерны более крупные однородные по форме частицы, чем для некапсулированного сухого экстракта, содержащего значительную долю пылевой фракции (твердые частицы различной формы размером < 50 мкм).
В результате проведенного сравнительного анализа показано, что микрокапсулы экстракта травы зюзника европейского имеют сферическую форму, гладкую поверхность, обладают хорошей сыпучестью и значительно отличаются по своим технологическим характеристикам (табл. 1, рис. 4) от сухого экстракта. Преимуществами микрокапсулированной формы экстракта являются его технологичность в процессе получения лекарственных препаратов и отсутствие гигроскопичности, свойственной субстанции растительного происхождения.
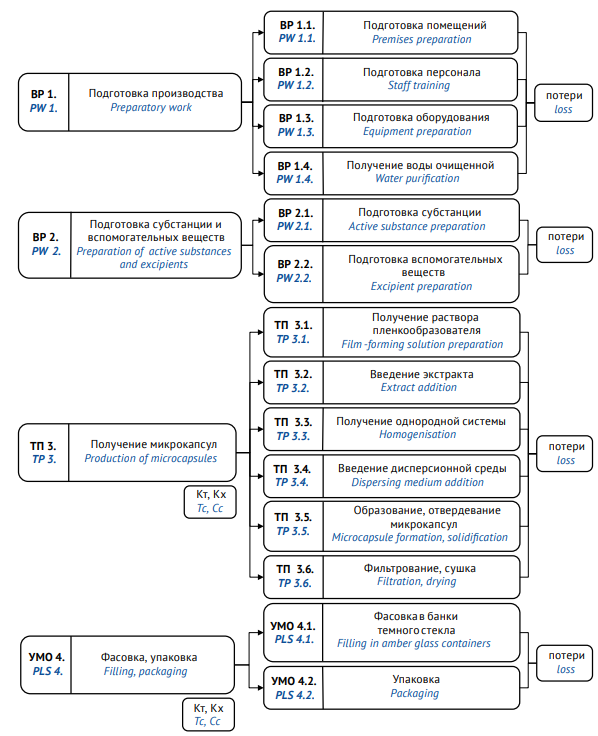
Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 1. Технологическая схема получения микрокапсул сухого экстракта травы зюзника европейского методом диспергирования. Кт — контроль технологический, Кх — контроль химический
Fig. 1. Process flow diagram for the production of microcapsules of Lycopus europaeus herb dry extract by dispersion. Tc, technological control; Cc, chemical control
Таблица 1. Физико-химические характеристики сухого экстракта травы зюзника европейского и микрокапсул экстракта
Table 1. Physicochemical properties of Lycopus europaeus herb dry extract and dry extract microcapsules
|
Характеристика Property |
Сухой экстракт Dry extract |
Микрокапсулы экстракта Dry extract microcapsules |
|
Размер частиц, мкм Particle size, μm |
10–100 |
50–300 |
|
Форма частиц Particle shape |
Пластины, параллелепипеды, овалы с неровными краями и бугристой поверхностью Plates, parallelepipeds, and ovals with uneven edges and bumpy surfaces |
Сферическая с гладкой поверхностью Spheres with smooth surfaces |
|
Влажность, % Moisture, % |
4,87±0,23 |
3,21±0,12 |
|
Качественный анализ (ТСХ) Identification (TLC) |
В сравнении с пятном розмариновой кислоты (Rf 0,33) Corresponds to the spot obtained with the rosmarinic acid standard (Rf 0.33) |
В сравнении с пятном розмариновой кислоты (Rf 0,33) Corresponds to the spot obtained with the rosmarinic acid standard (Rf 0.33) |
|
Угол естественного откоса, град. Angle of repose, deg. |
38±2 |
32±1 |
|
Сыпучесть (10 мм), г/с Flow through an orifice (10 mm), g/s |
0,00 |
5,24±0,21 |
|
Сыпучесть (10 мм) в режиме вибрации, г/с Flow through an orifice (10 mm) with vibration, g/s |
5,00±0,20 |
5,78±0,17 |
|
Сыпучесть (15 мм), г/с Flow through an orifice (15 mm), g/s |
0,00 |
10,53±0,23 |
|
Сыпучесть (15 мм) в режиме вибрации, г/с Flow through an orifice (15 mm) with vibration, g/s |
4,20±0,20 |
20,45±0,27 |
|
Насыпная плотность, г/мл до уплотнения Bulk density, g/mL после уплотнения Tapped density, g/mL |
0,6590±0,0140 0,7890±0,0200 |
0,5496±0,0161 0,6438±0,0055 |
Таблица составлена авторами по собственным данным / The table is prepared by the authors using their own data
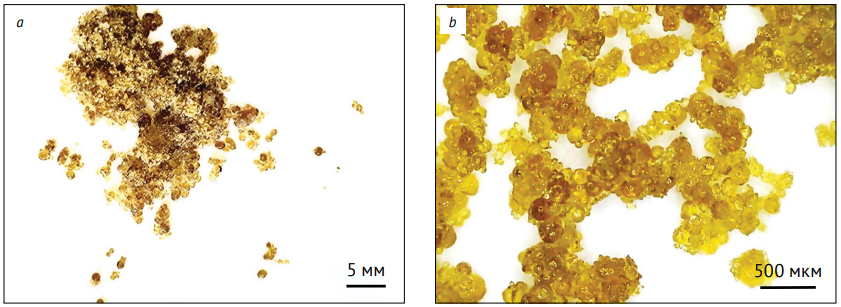
Фотография выполнена авторами / The photograph is taken by the authors
Рис. 2. Фотография микрокапсул сухого экстракта травы зюзника европейскогo при различном увеличении
Fig. 2. Microcapsules of Lycopus europaeus herb dry extract photographed at different magnifications
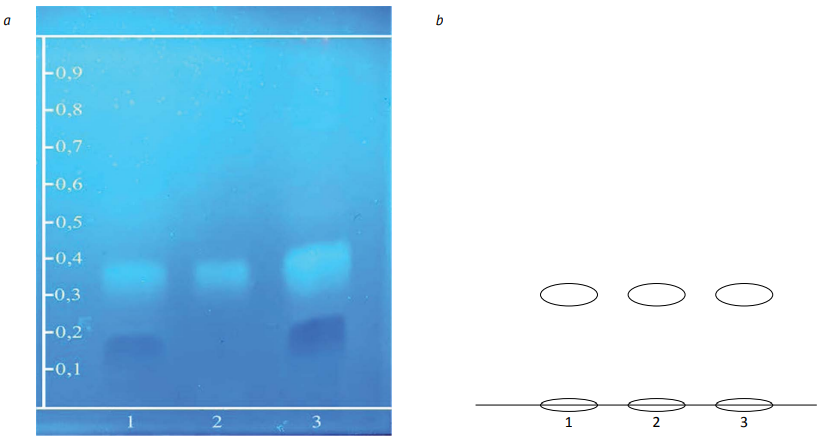
Рисунок подготовлен авторами по собственным данным / The figure is prepared by the authors using their own data
Рис. 3. Хроматограмма (а) экстракта травы зюзника европейского в ультрафиолетовом свете и схема хроматограммы (b): 1 — сухой экстракт травы зюзника европейского; 2 — стандартный образец розмариновой кислоты; 3 — микрокапсулы сухого экстракта травы зюзника европейского
Fig. 3. Chromatogram of Lycopus europaeus herb dry extract (1), rosmarinic acid standard (2), and microcapsules of Lycopus europaeus herb dry extract (3) in UV light (a) and as a scheme (b)
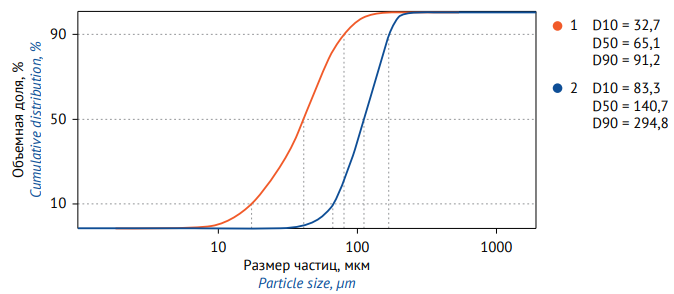
Рисунок подготовлен авторами по собственным данным / The figure is prepared by the authors using their own data
Рис. 4. Интегральное распределение частиц сухого экстракта травы зюзника европейского (1) и его микрокапсулированной формы (2) по размеру. D10, D50, D90 — размер частиц (мкм), соответствующий объемной доле 10, 50, 90% соответственно
Fig. 4. Cumulative curves of particle size distribution of Lycopus europaeus herb dry extract (1) and its microencapsulated form (2). D10, D50, and D90 are particle sizes (μm) corresponding to a volume fraction of 10, 50, and 90%, respectively
Заключение
Методом диспергирования получены микрочастицы сухого экстракта травы зюзника европейского, в качестве вспомогательного вещества использован желатин марки П-11. Проведена оценка качества полученных микрокапсул по следующим показателям: размер и форма микрочастиц, подлинность (методом тонкослойной хроматографии), эффективность инкапсулирования, влажность, угол естественного откоса, сыпучесть, насыпная плотность. Микрокапсулы экстракта представляют собой однородные частицы размером 50–300 мкм с влажностью 3,21±0,12%, хорошей сыпучестью. Эффективность инкапсулирования при использовании метода диспергирования достигает 95,0±1,3%, что позволяет сделать вывод о возможности использования разработанной технологии для получения микрокапсулированных лекарственных препаратов растительного происхождения.
1 Указ Президента Российской Федерации от 19.04.2017 № 176 «О Стратегии экологической безопасности Российской Федерации на период до 2025 года».
2 ГОСТ 12.1.007-76 Вредные вещества. Классификация и общие требования безопасности. М.; 1990.
3 ОФС.1.5.3.0007.15 Определение влажности лекарственного растительного сырья и лекарственных растительных препаратов. Государственная фармакопея Российской Федерации. XIV изд. Т. 2. М.; 2018.
4 ОФС.1.4.2.0016.15 Степень сыпучести порошков. Государственная фармакопея Российской Федерации. XIV изд. Т. 2. М.; 2018.
5 ОФС.1.2.1.0008.15 Определение распределения частиц по размеру методом лазерной дифракции света. Государственная фармакопея Российской Федерации. XIV изд. Т. 1. М.; 2018.
6 ОФС.1.1.0013.15 Статистическая обработка результатов химического эксперимента. Государственная фармакопея Российской Федерации. XIV изд. Т. 1. М.; 2018.
7 ГОСТ 11293-2017 Желатин. Технические условия. М.; 2020.
8 ОФС.1.4.1.0010.15 Порошки. Государственная фармакопея Российской Федерации. XIV изд. Т. 2. М.; 2018.
ОФС.1.4.1.0021.15 Экстракты. Государственная фармакопея Российской Федерации. XIV изд. Т. 2. М.; 2018.
Список литературы
1. Jităreanu A, Trifan A, Vieriu M, Caba I-C, Mârțu I, Agoroaei L. Current trends in toxicity assessment of herbal medicines: a narrative review. Processes. 2023;11(1):83. https://doi.org/10.3390/pr11010083
2. Крепкова ЛВ, Бабенко АН, Лемясева СВ, Боровкова МВ, Кузина ОС. Некоторые аспекты доклинического изучения безопасности зюзника европейского (Lycopus europaeus L.) экстракта сухого. Вопросы биологической, медицинской и фармацевтической химии. 2020;23(8):40–7. https://doi.org/10.29296/25877313-2020-08-06
3. Лупанова ИА, Крепкова ЛВ, Ферубко ЕВ, Трумпе ТЕ, Бортникова ВВ, Бабенко АН и др. Новые лекарственные средства растительного происхождения ВИЛАР. М.: ФГБНУ ВИЛАР; 2021. EDN: DJSFKW
4. Кузина ОС, Боровкова МВ, Крепкова ЛВ. Токсикологическая характеристика зюзника европейского (Lycopus europaeus L.) и зюзника высокого (Lycopus exaltatus L.) травы экстрактов сухих в условиях «острого» опыта. В кн.: Сборник трудов II Международной научной конференции «Роль метаболомики в совершенствовании биотехнологических средств производства». М.; 2019. С. 131–5. EDN: ECOXZM
5. Автина НВ, Писарев ДИ, Новиков ОО, Томчаковская ЕА, Безменова МД. Разработка состава и технологии микрокапсул с экстрактом черемухи поздней. Современные проблемы науки и образования. 2012;(4):304. EDN: PBITLF
6. Белошапкина ОМ, Семкина ОА. Разработка технологии получения микрокапсул сухого экстракта травы зюзника европейского (Lycopus europaeus L.). В кн.: Сборник трудов Х Международной научно-практической конференции молодых ученых «Современные тенденции развития технологий здоровьесбережения». Москва; 2022. С. 357–60. https://doi.org/10.52101/9785870191058_357
7. Семкина ОА, Джавахян МA, Белошапкина ОМ, Громакова АИ. Технологические аспекты получения микрокапсул субстанций растительного происхождения. Вопросы биологической, медицинской и фармацевтической химии. 2021;24(5):5–14. https://doi.org/10.29296/25877313-2021-05-01
8. Garg A, Chhipa K, Kumar L. Microencapsulation techniques in pharmaceutical formulation. Eur J Pharm Med Res. 2018;5(3):199–206.
9. Семкина ОА, Зверева ВИ, Джавахян МА, Хомик АС. Физико-химические и технологические характеристики зюзника европейского травы экстракта сухого и композиции на его основе. Химико-фармацевтический журнал. 2019;53(6):38–41. https://doi.org/10.30906/0023-1134-2019-53-6-38-41
10. Семкина ОА, Джавахян МА, Белошапкина ОМ, Борисенко ЕВ, Сидельников НИ. Способ инкапсуляции сухих растительных экстрактов. Патент Российской Федерации № 2782431; 2022.
Об авторах
О. А. СемкинаРоссия
Семкина Ольга Александровна, канд. фарм. наук
Ул. Грина, д. 7, стр. 1, Москва, 117216
О. М. Белошапкина
Россия
Белошапкина Ольга Михайловна
Ул. Грина, д. 7, стр. 1, Москва, 117216
Дополнительные файлы
Рецензия
Для цитирования:
Семкина О.А., Белошапкина О.М. Технология получения и оценка качества микрокапсул сухого экстракта травы зюзника европейского (Lycopus europaeus L.). Ведомости Научного центра экспертизы средств медицинского применения. Регуляторные исследования и экспертиза лекарственных средств. 2024;14(1):72-80. https://doi.org/10.30895/1991-2919-2023-575
For citation:
Semkina O.A., Beloshapkina O.M. Production Technology and Quality Assessment of Microcapsules of Lycopus europaeus L. Herb Dry Extract. Bulletin of the Scientific Centre for Expert Evaluation of Medicinal Products. Regulatory Research and Medicine Evaluation. 2024;14(1):72-80. (In Russ.) https://doi.org/10.30895/1991-2919-2023-575



































