Перейти к:
Роль и безопасность вспомогательных веществ в лекарственной форме «сиропы»: обзор
https://doi.org/10.30895/1991-2919-2025-15-2-190-205
Резюме
ВВЕДЕНИЕ. Сиропы являются важной лекарственной формой (ЛФ), применяющейся в том числе в педиатрической практике (на январь 2024 года в Российской Федерации зарегистрировано 212 лекарственных препаратов в форме сиропов). Эффективность, безопасность и качество этой ЛФ определяются составом лекарственного препарата (ЛП), в том числе вспомогательными веществами (ВВ).
ЦЕЛЬ. Анализ и систематизация данных о роли и безопасности вспомогательных веществ в составе лекарственной формы «сиропы», зарегистрированных в государственном реестре лекарственных средств Российской Федерации.
ОБСУЖДЕНИЕ. Рассмотрены основные группы ВВ, содержащихся в сиропах: подсластители, консерванты, растворители, загустители, модификаторы pH и буферные агенты, антиоксиданты и красители. Наиболее часто использующейся группой ВВ являются подсластители: сахароза (66,51%), сорбитол (29,25%), сахарин натрия (10,85%). Сахароза способствует развитию кариеса, а также противопоказана пациентам с сахарным диабетом и ожирением; сорбитол может вызывать желудочно-кишечные расстройства. Данные по безопасности искусственных подсластителей при длительном применении противоречивы, их выбор должен быть обоснован. Среди консервантов наиболее часто встречаются парабены: метилпарабен (31,60%) и пропилпарабен (20,28%). Пропилпарабен обладает потенциальной эстрогенной активностью, в связи с чем предпочтителен выбор метилпарабена. Растворители и сорастворители представлены водой, глицеролом (25,94%), этанолом (24,53%), пропиленгликолем (20,75%). Этанол и пропиленгликоль могут вызывать тяжелые нарушения со стороны центральной нервной системы. Наиболее часто используемым загустителем является гиэтеллоза (5,19%). Производные целлюлозы признаны безопасными, но их избыточное потребление может вызывать слабительный эффект. В качестве красителя наиболее часто применяется желтый «Солнечный закат» (7,54%). Данные по безопасности многих красителей недостаточны, что подчеркивает необходимость обоснованного подхода к их выбору.
ВЫВОДЫ. На основании анализа инструкций по медицинскому применению сиропов, зарегистрированных в ГРЛС, систематизированы данные о роли, безопасности и допустимых количествах ВВ в сиропах. Дана классификация и рассчитана частота встречаемости ВВ, входящих в состав сиропов. На основе выявленных данных предложено пересмотреть существующие подходы к выбору ВВ в сиропах, чтобы минимизировать потенциальные риски и повысить безопасность ЛП.
Ключевые слова
Для цитирования:
Косенко В.В., Новиков Я.С., Егорова С.Н., Евтеев В.А., Бунятян Н.Д. Роль и безопасность вспомогательных веществ в лекарственной форме «сиропы»: обзор. Регуляторные исследования и экспертиза лекарственных средств. 2025;15(2):190-205. https://doi.org/10.30895/1991-2919-2025-15-2-190-205
For citation:
Kosenko V.V., Novikov Ya.S., Egorova S.N., Evteev V.A., Bunyatyan N.D. Role and Safety of Excipients in Syrups (Review). Regulatory Research and Medicine Evaluation. 2025;15(2):190-205. (In Russ.) https://doi.org/10.30895/1991-2919-2025-15-2-190-205
ВВЕДЕНИЕ
Недостаток ассортимента лекарственных форм (ЛФ) для детей является важной проблемой здравоохранения во всем мире и одной из причин применения лекарственных препаратов (ЛП) не по назначению (off-label) [1], что сопряжено с высокими рисками [2]. Применение ЛП off-label варьирует от 3,3 до 94% в разных странах [1], в особенности в онкологии, психиатрии и при лечении редких заболеваний [3]. Педиатрическим комитетом Европейского агентства по лекарственным средствам (European Medicines Agency, EMA) были определены цели, направленные на устранение дефицита разнообразия ЛФ для детей1. Одна из приоритетных целей — разработка целевых педиатрических ЛФ [4].
Предпочтительными для употребления в педиатрии являются жидкие ЛФ, такие как растворы, сиропы и суспензии [5]. Большое значение играют вспомогательные вещества (ВВ), входящие в их состав, поскольку они способствуют сохранению качества препарата, его эффективности, а также приверженности пациентов к лечению. Безопасность применения ЛП в целом определяется в том числе безопасностью компонентов, входящих в его состав. Актуальной проблемой является недостаток данных о безопасности ВВ, входящих в состав ЛП для детей, а также их необоснованное применение [6].
В данной статье ВВ рассматриваются на примере одного из видов жидких ЛФ — сиропов. Сироп — ЛФ в виде водного раствора вязкой консистенции со сладким вкусом, содержащая сахарозу в концентрации не менее 45% или ее заменители, предназначенная для приема внутрь2. По данным Государственного реестра лекарственных средств (ГРЛС) России на январь 2024 года в России зарегистрировано 212 лекарственных препаратов в форме «сироп»3.
Сиропы обладают рядом преимуществ: простота приема, что особенно важно для детей, испытывающих трудности с проглатыванием таблеток или капсул; возможность индивидуального дозирования с помощью дозирующего устройства; маскировка неприятного вкуса активной фармацевтической субстанции и повышенная биодоступность в сравнении с твердыми ЛФ [5][7]. ВВ, входящие в состав сиропов, обеспечивают их стабильность, эффективность и приемлемость4.
Цель работы — анализ и систематизация данных о роли и безопасности вспомогательных веществ, использующихся в составе лекарственной формы «сиропы», зарегистрированных в государственном реестре лекарственных средств Российской Федерации.
Материалы исследования: инструкции по медицинскому применению 212 сиропов, зарегистрированных в ГРЛС, поисковая база данных объединенного экспертного комитета FAO/WHO (Food and Agriculture Organisation of the United Nations / World Health Organisation) по пищевым добавкам (Joint FAO / WHO Expert Committee on Food Additives, JECFA)5, база данных специального комитета по веществам, в целом признанным безопасными (Select Committee on GRAS (Generally Recognised As Safe) Substances database, SCOGS)6, список потенциально неподходящих ЛП в педиатрии [8], отчеты по безопасности EMA7, справочники по фармацевтическим вспомогательным веществам и научные публикации.
Поиск научных статей осуществлялся в базах данных Scopus, Pubmed, Google Scholar и eLIBRARY.RU по названию ВВ, входящих в состав сиропов, на английском и русском языках за период 2002–2024 гг.
Оценка профиля безопасности подсластителей проводилась на основе следующих параметров:
- допустимой нормы суточного потребления (acceptabledaily intake, ADI)8 путем анализа поисковой базы данных JECFA9;
- квалификации вещества по данным базы данных специального комитета по веществам, в целом признанным безопасными (SCOGSdatabase10). К безопасным относили вещества 1 и 2 типа заключений SCOGS.
Частоту встречаемости (Ч, %) рассчитывали по формуле (1):
Ч = ВВ/С×100, (1)
где ВВ — количество зарегистрированных в ГРЛС рецептур сиропов, содержащих исследуемое ВВ, С — количество сиропов, зарегистрированных на территории Российской Федерации.
ОСНОВНАЯ ЧАСТЬ
Классификация вспомогательных веществ
Все ВВ, входящие в состав сиропов, можно классифицировать по природе происхождения (рис. 1) и по назначению (табл. 1).
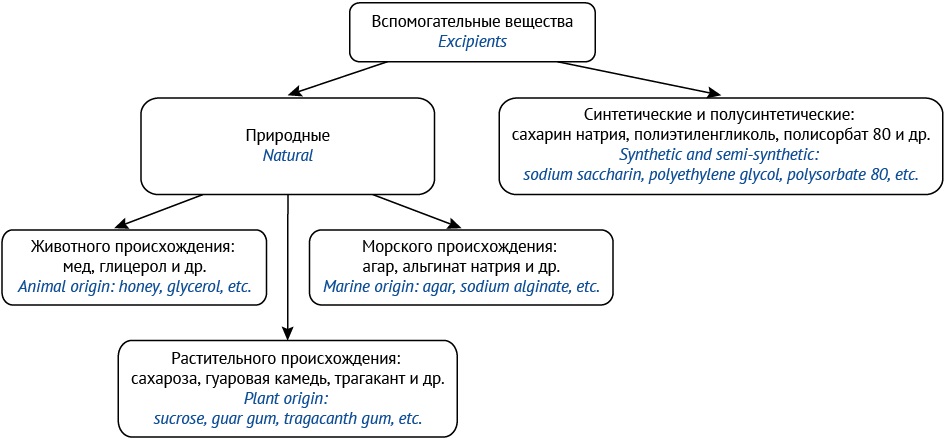
Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 1. Классификация вспомогательных веществ по природе происхождения
Fig. 1. Classification of excipients by origin
Таблица 1. Классификация вспомогательных веществ по назначению
Table 1. Classification of excipients by purpose
Группа вспомогательных веществ по назначению Group of excipients by purpose | Вспомогательные вещества Excipients |
Подсластители Sweeteners | Аспартам, ацесульфам калия, глюкоза (декстроза), ксилитол (ксилит), мальтитол (мальтит), неогесперидина дигидрохалкон, сахарин натрия (сахаринат натрия), сахароза, сироп инвертированный, сорбитол (сорбит), сукралоза, цикламат натрия Aspartame, acesulfame potassium, glucose (dextrose), xylitol, maltitol, neohesperidin dihydrochalcone, sodium saccharin, sucrose, invert syrup, sorbitol, sucralose, sodium cyclamate |
Ароматизаторы Flavours | Масла: анисовое, апельсиновое, гвоздики, коричное, мяты перечной, розы, фенхельное, базиликовое. Прочие: абрикосовый, американское мороженое, ананасовый, анетол, апельсиновый, аронии плодов сок концентрированный, банановый, ванилин, ваниль с натуральным экстрактом rx15460, вишневый, грейпфрутовый, грушевый, дыня, карамель-крем 761, каштана листьев экстракт густой спиртовой, клубника с натуральным экстрактом rx9711, клубничный, кремовый, лесные ягоды r3712-1, лимонный, малиновый, мед натуральный, медовый, ментол, мятно-анисовый, персиковый, розовый, сладкий апельсин, сливовый, сливочный, тутти-фрутти, фенхельный, фруктовый, цитрусовый, черносмородиновый, шоколадная ваниль Oils: anise, orange, clove, cinnamon, peppermint, rose, fennel, basil Other: menthol, apricot, American ice cream, pineapple, anethole, orange, chokeberry fruit juice concentrate, banana, vanillin, vanilla (with natural extract) RX 15460, cherry, grapefruit, pear, melon, caramel cream 761, soft alcoholic extract of chestnut leaf, strawberry (with natural extract) RX 9711, strawberry, cream, wild berries R3712-1, lemon, raspberry, natural honey, honey, menthol, mint-anise, peach, pink, sweet orange, plum, creamy, tutti-frutti, fennel, fruity, citrus, blackcurrant, chocolate vanilla |
Красители Colourants | BQ супра, азорубин, бета-каротин, желтый «Солнечный закат», карамель, колер эликсирный, патентованный синий, пунцовый 4R, рибофлавин, тропеолин 00, хинолиновый желтый, экстракт свеклы BQ Supra, azorubine, beta-carotene, Sunset Yellow, caramel colouring, elixir colour, Patent Blue, Ponceau 4R, riboflavin, Tropaeolin 00, Quinoline Yellow, beetroot extract |
Консерванты Preservatives | Парабены: метилпарабен, пропилпарабен, бутилпарабен Бензойная кислота и ее производные: бензойная кислота, бензоат натрия Сорбиновая кислота и ее производные: сорбиновая кислота и сорбат калия Parabens: methylparaben, propylparaben, butylparaben Benzoic acid and its derivatives: benzoic acid, sodium benzoate Sorbic acid and its derivatives: sorbic acid and potassium sorbate |
Модификаторы pH и буферные агенты pH modifiers and buffering agents | Лимонная кислота безводная, лимонной кислоты моногидрат, молочная кислота, натрия ацетат, натрия гидроксид, натрия гидрофосфат, натрия цитрат дигидрат, натрия цитрат пентасексвигидрат, уксусная кислота ледяная, хлористоводородная кислота разведенная, цитрат натрия Anhydrous citric acid, citric acid monohydrate, lactic acid, sodium acetate, sodium hydroxide, sodium hydrogen phosphate, sodium citrate dihydrate, trisodium citrate 5.5-hydrate, glacial acetic acid, diluted hydrochloric acid, sodium citrate |
Модификаторы вязкости (загустители) Viscosity modifiers (thickeners) | Агар, алгинат натрия, гидроксиэтилцеллюлоза, гипромеллоза, гуаровая камедь, диметилполисилоксан, кармеллоза натрия, кремний очищенный, ксантановая камедь, трагакантовая камедь Agar, sodium alginate, hydroxyethylcellulose, hypromellose, guar gum, dimethylpolysiloxane, carmellose sodium, purified silicon, xanthan gum, tragacanth gum |
Растворители и сорастворители Solvents and co-solvents | Вода, глицерол, пропиленгликоль, этанол Water, glycerol, propylene glycol, ethanol |
Антиоксиданты Antioxidants | Аскорбиновая кислота, динатрия эдетат Ascorbic acid, disodium edetate |
Таблица составлена авторами / The table is prepared by the authors
Подсластители
Основной группой ВВ, использующихся при производстве сиропов, являются подсластители, улучшающие вкус лекарственного препарата (табл. 2).
Таблица 2. Основные характеристики подсластителей, входящих в состав сиропов, зарегистрированных на территории Российской Федерации
Table 2. Main characteristics of sweeteners included in syrups approved in the Russian Federation
Наименование Name | Количество13 Quantity13 | Происхождение [9] Origin [9] | Сладость [9] Sweetness [9] | Гликемический индекс [10] Glycaemic index [10] | Калорийность, ккал/г [10] Caloric content, kcal/g [10] | ADI, мг/кг массы тела в сутки14 ADI, mg/kg body weight per day14 | GRAS15 |
Сахароза / Sucrose | 141 | Натуральный Natural | 1 | 60 | 4,0 | – | + |
Сорбитол / Sorbitol | 62 | 0,6 | 9 | 2,5 | – | + | |
Мальтитол / Maltitol | 7 | 0,9 | 36 | 2,7 | – | – | |
Глюкоза / Glucose | 6 | 0,74 | 100 | 3,4 | – | + | |
Сироп инвертированный / Inverted syrup | 5 | 1,3 | 60 | – | – | – | |
Подсластитель натуральный* / Natural sweetener* | 1 | – | – | – | – | – | |
Сахарин натрия / Sodium saccharin | 23 | Синтетический Artificial | 300–500 | 0 | 0 | 0–5 | – |
Ацесульфам К / Acesulfame K | 3 | 130–200 | 0 | 0–15 | – | ||
Цикламат натрия / Sodium cyclamate | 2 | 30 | 0 | 0–11 | – | ||
Сукралоза / Sucralose | 2 | 400–800 | 0 | 0–15 | – | ||
Аспартам / Aspartame | 1 | 180–200 | 4,0 | 0–40 | – | ||
Неогесперидина дигидрохалкон / Neohesperidin dihydrochalcone | 1 | 1500–1800 | 2,0 | – | – | ||
Итого / Total | 254 |
Таблица составлена авторами / The table is prepared by the authors
Примечание. «Количество» — количество зарегистрированных в ГРЛС рецептур сиропов, содержащих исследуемое ВВ; «сладость» — сладость в сравнении с сахарозой; ADI — допустимая норма суточного потребления; GRAS — список веществ, общепризнанных безопасными; «+» — вещество входит в базу данных SCOGS, «–» — ВВ отсутствует в базах данных.
* Состав подсластителя натурального в инструкции по медицинскому применению ЛП не раскрывается.
Note. ‘Quantity’ stands for the number of syrup formulations containing the excipient of interest that are registered in the State Register of Medicines. ‘Sweetness’ means sweetness compared with sucrose. ADI, acceptable daily intake; GRAS, list of substances generally recognised as safe. The substances marked with ‘+’ are included in the Select Committee on GRAS Substances (SCOGS) database, and those marked with ‘–’ are not in the database.
* The composition of the natural sweetener is not disclosed in the summary of product characteristics.
Подсластители в сиропах можно разделить на две основные группы: натуральные и синтетические. Синтетические подсластители зачастую в сотни раз слаще сахарозы [9]. По другой классификации выделяют калорийные (высококалорийные (сахароза, глюкоза, инвертированный сироп) и низкокалорийные (сорбитол, мальтитол)) и некалорийные (сахарин, ацесульфам К, цикламат, сукралоза, неогеспередина дигидрохалкон) подсластители. К некалорийным подсластителям также принято относить аспартам, хотя его калорийность составляет 4 ккал/г, так как он используется в малых количествах11. Считается, что использование низкокалорийных и некалорийных подсластителей предотвращает кариес зубов и ожирение [9][11], они могут быть использованы пациентами с сахарным диабетом [12].
Как правило, в состав сиропов входят натуральные подсластители (87%), среди которых чаще всего (66,51%) встречается сахароза — натуральный дисахарид, состоящий из остатков моносахаридов: α-глюкозы и β-фруктозы. Наибольшую физическую и химическую стабильность сахароза проявляет в диапазоне pH от 4 до 8. Во флаконах, содержащих сахарозу, наблюдается эффект «запирания крышки», вызванный кристаллизацией сахарозы на крышке и горлышке флакона12 [13]. Для предотвращения такого явления сахарозу используют в комбинации с сахарными спиртами (полиолами) и/или глицеролом. В высоких концентрациях сахарозу используют в качестве консерванта, а также для повышения вязкости раствора [14]. Сахароза представляет собой наиболее кариесогенный подсластитель, так как вызывает снижение pH зубного налета и реминерализацию зубной эмали [15], в связи с чем ее не рекомендуется использовать в детских сиропах [9][16]. Кроме того, она противопоказана пациентам с сахарным диабетом и ожирением [11][15].
Из натуральных калорийных подсластителей также применяются глюкоза (декстроза) и инвертированный сироп. Глюкоза также добавляется в сиропы для регулирования вязкости [9]. Инвертированный сироп представляет собой смесь моносахаридов глюкозы и фруктозы, получаемых из сахарозы. Глюкоза и инвертированный сироп, так же как и сахароза, являются кариесогенными, высококалорийными и противопоказаны пациентам с сахарным диабетом. Эти подсластители не нашли широкого применения и встречаются в составе сиропов в 2,83 и 2,36% случаев соответственно.
В состав сиропов часто (32,55% сиропов) входят сахарные спирты (полиолы). Они разделяются на производные моносахаридов (сорбитол); производные дисахаридов (мальтитол) или смеси производных полисахаридов (сироп мальтитола) [9].
Сорбитол (сорбит, E420) содержится в 29,25% сиропов и представляет собой шестиуглеродный полиол cо сладким охлаждающим вкусом и горьким послевкусием [17][18]. Сорбитол относительно стабилен и совместим со многими ВВ. В сиропах он эффективно предотвращает кристаллизацию вокруг крышки бутылки [18][19]. Сорбитол считается безопасным для взрослых и детей, поскольку не всасывается в пищеварительном тракте [16]. Он также признается менее кариесогенным, поскольку слабо ферментируется бактериями в полости рта [9] и лучше переносится пациентами с сахарным диабетом [20]. Сорбитол может вызывать желудочно-кишечные расстройства, такие как боль в животе, метеоризм, рвота, вздутие живота при приме от 5 до 20 г [16][21]. В высоких количествах (более 20 г в сутки для взрослых) оказывает слабительное действие [21]. Кроме того, потребления сорбитола следует избегать пациентам с непереносимостью фруктозы [16].
Мальтитол (мальтит, Е965) представляет собой дисахаридный полиол, состоящий из глюкозы и сорбитола в равных частях. Он не подвергается процессам карамелизации и потемнения, а его охлаждающий эффект незначителен по сравнению с другими полиолами [18]. Мальтитол встречается в сиропах только в 3,3% случаев несмотря на то, что считается безопасным. Как и другие полиолы, он обладает малой кариесогенностью, но по сравнению с ними имеет высокий гликемический индекс. В больших количествах мальтитол может вызывать метеоризм и диарею [9][18][19].
Синтетические подсластители содержатся в 13% сиропов. Они обладают сильной подслащивающей способностью, поэтому используются для замены натуральных подсластителей. Считается, что синтетические подсластители более безопасны и могут применяться пациентами с ожирением и сахарным диабетом [12], являются некалорийными и не выступают источником энергии для бактерий полости рта, в связи с чем считаются некариесогенными [9]. Следует отметить, однако, что употребление синтетических подсластителей с раннего возраста может привести к нарушению чувствительности к сладкому, что может увеличить сердечно-сосудистый риск и общую смертность [12].
Наиболее часто использующимся синтетическим подсластителем (10,85%) (третий по распространенности среди всех подсластителей) является сахарин натрия (сахаринат натрия, E954) — производное о-сульфабензамида. Он используется в концентрации 0,02–0,5%, имеет очень сладкий вкус с металлическим или горьким послевкусием, для маскировки которого его комбинируют с другими подсластителями [22]. Ранее считалось, что сахарин натрия — потенциальный канцероген и может вызывать рак мочевого пузыря, однако данные предположения не подтвердились [23]. Следует, однако, учесть, что сахарин натрия может вызывать крапивницу, зуд, фотосенсибилизацию, экзему, а также тошноту и диарею [16].
Ацесульфам калия (ацесульфам К, E950) представляет собой калиевую соль 6-метил-1,2,3-оксатиазин-4(3H)-она 2,2-диоксида. Ацесульфам калия встречается в 1,42% сиропов, зарегистрированных в ГРЛС, также обладает горьким послевкусием в высоких количествах [12]. Он не метаболизируется в организме, выводится почками в неизмененном виде [24] и в целом признан безопасным, однако данные противоречивы [23][25].
Сукралоза (1’,4’,6’-трихлоргалактосахароза, E955) — синтетический подсластитель, представляющий собой замещенный дисахарид, аналогичный сахарозе, в котором 3 гидроксильные группы замещены 3 атомами хлора [26]. Содержится только в 0,94% сиропов, представленных в ГРЛС. Сукралоза не метаболизируется в организме и выводится в неизменном виде [15]. Многочисленные исследования демонстрируют безопасность использования сукралозы [26], однако она может увеличить экспрессию белка-транспортера гликопротеина P и двух изоформ цитохрома P450, участвующих в метаболизме ЛС [16].
Цикламат натрия (натриевая соль цикламовой кислоты, E952) — синтетический некалорийный подсластитель, входит в состав 0,94% сиропов, представленных в ГРЛС. Он слаще сахара всего лишь в 30 раз и имеет горькое послевкусие, что делает его наименее предпочтительным среди синтетических подсластителей [23]. Цикламат натрия метаболизируется в кишечнике до циклогексиламина, который может вызывать нарушения со стороны сердечно-сосудистой и нервной систем [23–25].
Аспартам (L-аспартил-L-фенилаланин, Е951) представляет собой дипептид, состоящий из аспарагиновой кислоты и метилового эфира фенилаланина; не обладает горьким послевкусием [12], представлен только в одном сиропе. Фенилаланин в составе аспартама представляет собой угрозу для пациентов с фенилкетонурией, а также для беременных женщин, вынашивающих плод с таким нарушением [16][23]. Существует достаточно научных доказательств, подтверждающих, что аспартам безопасен для потребления в максимально допустимой норме суточного потребления [16][27]. Среди нежелательных эффектов аспартама отмечают неврологические (нейротоксичность, эпилепсия, головная боль, панические атаки и галлюцинации) и реакции гиперчувствительности. Несмотря на то что Международное агентство по изучению рака (International Agency for Research on Cancer, IARC) классифицировало аспартам как возможно канцерогенный для человека (группа 2B)16 на основании ограниченных данных о раке у людей (в частности, гепатоцеллюлярной карциноме — разновидности рака печени), он до сих пор применяется в фармации.
Таким образом, подсластители играют важную роль в улучшении вкуса сиропов, но их использование в педиатрической практике должно быть обоснованным. Несмотря на широкое применение сахарозы в детских сиропах, целесообразность ее использования вызывает сомнения из-за высокого риска развития кариеса и противопоказаний для пациентов с сахарным диабетом и ожирением. Более безопасными альтернативами являются сорбитол и мальтитол, характеризующиеся низкой кариесогенностью и безопасностью для пациентов с диабетом. Важно также учитывать возможность комбинирования подсластителей для снижения их доз и минимизации побочных эффектов, что позволит создать более безопасные и универсальные составы сиропов.
Консерванты
Введение консервантов в состав ЛП позволяет продлить срок годности сиропа (табл. 3).
Таблица 3. Основные характеристики консервантов, входящих в состав сиропов, зарегистрированных на территории Российской Федерации
Table 3. Main characteristics of preservatives included in syrups approved in the Russian Federation
Наименование Name | Количество24 Quantity24 | ADI, мг/кг массы тела в сутки25 ADI, mg/kg body weight per day25 | GRAS26 | Оптимальный pH Optimum pH |
Метилпарабен / Methylparaben | 67 | 0–10 | + | 4,5–7,5 |
Пропилпарабен / Propylparaben | 43 | – | + | 3,0–8,0 |
Бензоат натрия / Sodium benzoate | 41 | 0–5 | + | 2,5–4,0 |
Сорбат калия / Potassium sorbate | 13 | 0–25 | + | 2,0–6,5 |
Бензойная кислота / Benzoic acid | 12 | 0–5 | + | 2,5–4,0 |
Сорбиновая кислота / Sorbic acid | 8 | 0–25 | + | 4,0–6,0 |
Бронопол / Bronopol | 2 | – | – | 5,0–8,8 |
Бутилпарабен / Butylparaben | 1 | – | – | 3,0–6,0 |
Итого / Total | 187 |
Таблица составлена авторами по данным Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017 / The table is prepared by the authors using data from Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017
Примечание. Количество — количество зарегистрированных в ГРЛС рецептур сиропов, содержащих исследуемое ВВ; ADI — допустимая норма суточного потребления, GRAS — список веществ, общепризнанных безопасными, «+» — вещество входит в базу данных SCOGS, «–» — ВВ отсутствует в базе данных.
Note. ‘Quantity’ stands for the number of syrup formulations containing the excipient of interest that are registered in the State Register of Medicines. ADI, acceptable daily intake; GRAS, list of substances generally recognised as safe. The substances marked with ‘+’ are included in the Select Committee on GRAS Substances (SCOGS) database, and those marked with ‘–’ are not in the database.
Чаще всего в сиропах встречаются парабены — алифатические эфиры пара-гидроксибензойной кислоты [28]: метилпарабен (метилпарагидроксибензоат, нипагин, E218), пропилпарабен (пропилпарагидроксибензоат, нипазол, E216), бутилпарабен (бутилпарагидроксибензоат). Они не имеют запаха и вкуса, что делает их предпочтительными для включения в состав ЛП для перорального приема [29]. Растворимость парабенов снижается, а противомикробные свойства увеличиваются с увеличением алифатической цепи (от метилпарабена к бутилпарабену) [28]. Парабены проявляют наибольшую активность в диапазоне pH от 4 до 8, эффективно подавляя рост грамположительных бактерий и оказывая ингибирующее действие на грибы, в том числе плесневые [30]. Метилпарабен может быть использован индивидуально в концентрациях от 0,015 до 0,2%, однако чаще в состав ВВ вводят смесь метилпарабена и пропилпарабена в пропорции 9 : 1 (0,18% метилпарабена + 0,02% пропилпарабена)17. Пропилпарабен также может быть использован в чистом виде в концентрациях 0,02–0,06%18, бутилпарабен — в концентрации 0,006–0,05%19. Метилпарабен, пропилпарабен и бутилпарабен входят в состав 31,60, 20,28 и 0,47% сиропов, зарегистрированных в ГРЛС, соответственно.
EMA утверждает, что метилпарабен до 0,2% (2,8 мг/кг/сут) в ЛП для перорального применения безопасен для взрослых и детей любого возраста. Применение пропилпарабена вызывает настороженность, поскольку это вещество обладает определенной эстрогенной активностью. Допустимо применение пропилпарабена в количестве, не превышающем 0,06% (1 мг/кг/сут)20. Следует отметить, что объединенный экспертный комитет FAO/WHO по пищевым добавкам исключил допустимую суточную дозу (до 10 мг/кг/сут) для пропилпарабена в связи с неблагоприятным воздействием на ткани репродуктивных органов у самцов крыс21. В целом парабены считаются безопасными, но могут вызывать гипербилирубинемию, реакции гиперчувствительности, эстрогенные эффекты (пропилпарабен) и контактный дерматит замедленного типа22. Также парабены могут вызывать реакцию перекрестной гиперчувствительности у пациентов с аллергией на аспирин [16]. Согласно KIDs List метилпарабен и пропилпарабен могут вызывать ядерную желтуху у новорожденных, поэтому не рекомендуется их применение у детей младше 2 мес. [8].
Вторыми по частоте применения консервантами в сиропах являются производные бензойной кислоты. Широко применяется (19,34% сиропов) бензоат натрия (Е211) в концентрации 0,02–0,5% [16]. Он легко растворим в воде, не имеет запаха и вкуса [31], обладает бактериостатическим и противогрибковым действием и наиболее активен при pH 2–523. Считается, что бензоат натрия в допустимых дозах является безопасным, так как не накапливается в организме. В больших количествах может вызывать аллергические реакции [31].
Бензойная кислота (Е210) (частота встречаемости 5,66%) обладает похожими свойствами, но является менее растворимой в воде. Она также наиболее активна в кислой среде (рН 4,5) и обладает бактериостатическим действием. Бензойная кислота может вызывать крапивницу и другие аллергические реакции, является раздражителем слизистой желудка и кожи27. Учитывая возможные нежелательные реакции, EMA запрещает использование производных бензойной кислоты в терапии новорожденных и рекомендует применять их с осторожностью у детей старше 4 нед.28 KIDs List рекомендует избегать применение производных бензойной кислоты в дозировке 99 мг/кг/сут у новорожденных в связи с тем, что они могут вызывать гаспинг-синдром (синдром резкого удушья) [8].
Сорбат калия (E200) — антимикробный консервант, обладающий выраженными противогрибковыми и в меньшей степени антибактериальными свойствами (6,13% составов зарегистрированных сиропов). Чаще всего сорбат калия применяется в концентрации 0,1–0,2%. Он лучше растворяется в воде и более стабилен в водном растворе, чем сорбиновая кислота, в связи с чем чаще используется29. Сорбиновая кислота (входит в состав 3,77% сиропов) применяется в концентрациях от 0,05 до 0,2%. Оптимальная антимикробная активность сорбиновой кислоты достигается при pH 4,5. Ограниченное применение сорбиновой кислоты и ее калиевой соли в сиропах обуславливается низкой противомикробной активностью указанных консервантов при pH выше 6,0 и их несовместимостью со многими АФС30. Сорбат калия и сорбиновая кислота в допустимой суточной дозе считаются одними из наименее токсичных консервантов и практически не вызывают побочных эффектов [32].
Бронопол — антимикробный консервант, эффективный против грамположительных и грамотрицательных бактерий [33], используется в концентрациях от 0,01 до 0,1%. Бронопол не получил широкого распространения и встречается в составе только двух сиропов от кашля индийского производства. Известно его применение в качестве консерванта в составе ЛФ для наружного применения, но нет никаких данных о его применении в пероральных ЛФ31. Установлено, что бронопол нестабилен в щелочных условиях и разлагается на нитрометан, оксид азота(I), бромистый водород, муравьиную кислоту и метанол [33]. Известна способность бронопола выделять формальдегид и нитриты при разложении и совместно с аминами образовывать высокотоксичные нитрозамины32.
Роль спиртов/полиолов (глицерола, пропиленгликоля и этанола) в качестве консервантов рассмотрена в разделе «Сорастворители».
По нашему мнению, следует по возможности избегать добавления консервантов в сиропы, особенно в ЛП для детей, ввиду повышенного риска нежелательных реакций, включая гиперчувствительность и токсикологическую нагрузку на организм. В тех случаях, когда консервант необходим для сохранения длительного срока хранения, следует отдавать предпочтение более безопасным альтернативам, таким как сорбат калия и бензоат натрия, которые обладают хорошей антимикробной активностью и минимальной токсичностью. Однако даже эти консерванты должны использоваться с осторожностью у младенцев и пациентов с аллергией.
Сорастворители
Сорастворители повышают растворение плохо растворяющихся в воде фармацевтических субстанций и ВВ. Основные характеристики сорастворителей представлены в таблице 4.
Таблица 4. Основные характеристики вспомогательных веществ, входящих в состав сиропов, зарегистрированных на территории Российской Федерации
Table 4. Main characteristics of excipients included in syrups approved in the Russian Federation
Наименование Name | Количество38 Quantity38 | ADI мг/кг массы тела в сутки39 ADI, mg/kg body weight per day39 | GRAS40 |
Сорастворители / Co-solvents | |||
Глицерол / Glycerol | 55 | – | + |
Этанол / Ethanol | 52 | – | – |
Пропиленгликоль / Propylene glycol | 44 | 0–25 | + |
Итого / Total | 151 | ||
Антиоксиданты / Antioxidants | |||
Динатрия эдетат* / Disodium edetate* | 10 | 0–25 | + |
Аскорбиновая кислота / Ascorbic acid | 3 | – | + |
Итого / Total | 13 | ||
Загустители / Thickeners | |||
Гидроксиэтилцеллюлоза / Hydroxyethyl cellulose | 11 | – | – |
Ксантановая камедь / Xanthan gum | 7 | – | – |
Кармеллоза натрия / Carmellose sodium | 3 | – | + |
Альгинат натрия / Sodium alginate | 2 | – | + |
Глицерина оксистеарат / Glycerol oxystearate | 1 | – | – |
Агар / Agar | 1 | – | + |
Гидроксипропилметилцеллюлоза / Hydroxypropyl methylcellulose | 1 | – | + |
Трагакантовая камедь / Tragacanth gum | 1 | – | + |
Диметилполисилоксан / Dimethylpolysiloxane | 1 | 0–1,5 | – |
Гуаровая камедь / Guar gum | 1 | – | + |
Повидон / Povidone | 1 | 0–50 | – |
Кремния диоксид коллоидный / Colloidal silicon dioxide | 1 | – | + |
Итого / Total | 31 | ||
Красители / Colourants | |||
Желтый «Солнечный закат» / Sunset Yellow | 16 | 0–4 | - |
Карамель / Caramel | 10 | – | + |
Пунцовый 4R / Ponceau 4R | 7 | 0–4 | – |
BQ Супра / BQ Supra | 2 | – | – |
Тропеолин 00 / Tropaeolin 00 | 2 | – | – |
Рибофлавин / Riboflavin | 1 | – | + |
Экстракт свеклы / Beetroot extract | 1 | – | – |
Бета-каротин / Beta-carotene | 1 | – | + |
Хинолиновый желтый / Quinoline Yellow | 1 | 0–3 | – |
Итого / Total | 41 | ||
Таблица составлена авторами / The table is prepared by the authors
Примечание. «Количество» — количество зарегистрированных в ГРЛС рецептур сиропов, содержащих исследуемое ВВ; ADI — допустимая норма суточного потребления, GRAS — список веществ, общепризнанных безопасными; «+» — вещество входит в базу данных SCOGS; «–» — ВВ отсутствует в базе данных.
* Ввиду почти полного отсутствия биологических исследований Специальный комитет по веществам, в целом признанными безопасными, не имеет достаточных данных для оценки безопасности вещества (вещество отнесено к 5 типу SCOGS).
Note. ‘Quantity’ stands for the number of syrup formulations containing the excipient of interest that are registered in the Russian State Register of Medicines. ADI, acceptable daily intake; GRAS, list of substances generally recognised as safe. The substances marked with ‘+’ are included in the Select Committee on GRAS Substances (SCOGS) database, and those marked with ‘–’ are not in the database.
* Due to the almost complete lack of biological studies, the SCOGS does not have sufficient data to assess the safety of this substance (the substance is classified as SCOGS Type 5).
Глицерол (глицерин, E422) — прозрачная, бесцветная, без запаха, вязкая, гигроскопичная жидкость; имеет сладкий вкус, примерно в 0,6 раза слаще сахарозы [34]; является веществом многоцелевого назначения. В сиропах глицерол может применяться в качестве сорастворителя, консерванта, загустителя, подсластителя. В качестве консерванта и подсластителя используется в сиропах в концентрациях менее 20%33. Также глицерол входит в состав некоторых сиропов в качестве средства, смягчающего и увлажняющего кашель [35]. Частота встречаемости глицерола в составе сиропов составляет 25,94%. Глицерол содержится в тканях человека, поэтому считается безопасным [34]. В небольших количествах обладает легким слабительным действием. В концентрациях более 40% из-за гигроскопических и осмотических свойств может вызывать мукозит, а также диарею и электролитные нарушения. Среди взрослого населения глицерол редко вызывает побочные эффекты, однако в педиатрической практике были зарегистрированы случаи неврологической токсичности [16]. Глицерол не входит в KIDs List [8].
Пропиленгликоль является вторым по распространенности сорастворителем и добавляется в каждый пятый сироп (20,75%). Он применяется также в качестве консерванта (в концентрации 15–30%), загустителя и стабилизатора. Антимикробная активность пропиленгликоля сопоставима с этанолом, а активность против плесневых грибов схожа с глицеролом и лишь немного уступает этанолу34. Пропиленгликоль может поражать центральную нервную систему, особенно у новорожденных и детей до 4 лет. Из-за физиологической и метаболической незрелости детей пропиленгликоль может быстро накапливаться, вызывая токсичность [16]. Среди побочных эффектов отмечаются: лактоацидоз, угнетение центральной нервной системы (депрессия, кома, судороги), кардиотоксичность (аритмия, гипотензия), угнетение дыхания, одышка, гипогликемия, гемолиз и гемоглобинурия, нарушение функции почек (острый тубулярный некроз, острая почечная недостаточность)35 [8][16]. Рекомендуемые дозы пропиленгликоля в жидких ЛФ: для новорожденных (до 28 сут) — 1 мг/кг/сут, детям от 1 мес. до 4 лет — 50 мг/кг/сут, детям от 5 до 17 лет — 500 мг/кг/сут36. Входит в KIDs List, согласно которому рекомендуется избегать применения пропиленгликоля у новорожденных в дозах выше 3 г/сут, а также с осторожностью применять дозы свыше 34 мг/кг/сут [8].
Этанол (этиловый спирт) широко используется в сиропах (24,52% составов) в качестве сорастворителя и консерванта, может входить в состав препаратов, применяющихся с младенческого возраста (отхаркивающие сиропы солодки и алтея). В качестве консерванта используется в концентрациях не более 10%37. Добавление этанола в детские сиропы вызывает большую обеспокоенность, так как он может вызывать гипогликемию, лактоацидоз, тахикардию, гипотермию, нарушение сознания [36], может привести к ступору, коме, угнетению дыхания и сердечно-сосудистому коллапсу, гипогликемическим судорогам [16]. Согласно KIDs List, рекомендуется применять ЛП, содержащие этанол, с осторожностью в возрасте до 6 лет; в максимально допустимой концентрации 5% и под наблюдением врачей [8]. Управление по контролю за качеством продуктов питания и лекарственных средств (Food and Drug Administration, FDA) регламентирует содержание этанола в безрецептурных ЛП для перорального применения в зависимости от возраста: для взрослых и детей старше 12 лет — не более 10%, для детей от 6 до 12 лет — не более 5%, для детей до 6 лет — не более 0,5% [37].
Таким образом, несмотря на высокие риски токсичности, этанол широко применяется в детских сиропах, особенно в отхаркивающих средствах. Пропиленгликоль также требует осторожности, особенно у детей младше 4 лет. Глицерол, имеющий различное назначение в составе ВВ, может стать более безопасной альтернативой. Мы рекомендуем минимизировать или полностью исключить сорастворители из состава сиропов для детей, а при невозможности рассмотреть переход на другие ЛФ, такие как порошки или гранулы для приготовления раствора, которые не требуют добавления потенциально опасных ВВ.
Антиоксиданты
В составе сиропов антиоксиданты, такие как аскорбиновая кислота и динатрия эдетат, используются в концентрации менее 0,2%. Основные характеристики антиоксидантов представлены в таблице 4.
Аскорбиновая кислота чаще всего используется в сиропах шиповника как источник витамина С. Частота встречаемости — 1,42%. Побочных эффектов не выявлено.
Динатрия эдетат (динатриевая соль этилендиаминтетрауксусной кислоты, динатрия ЭДТА) является антиоксидантом и хелатирующим агентом, который широко применяется для связывания ионов металлов. Он образует прочные комплексы с Mn, Cu, Fe, Co. Известно применение динатрия ЭДТА в качестве консерванта [38][39]. В сиропах используется в концентрациях от 0,0125 до 0,1%; входит в состав противоаллергических сиропов с дезлоратадином и сиропов от кашля, содержащих амброксол. Частота встречаемости — 4,72%. Имеются данные о нефротоксичности и побочных эффектах со стороны желудочно-кишечного тракта при приеме солей ЭДТА, однако в целом он признан безопасным [39].
Использование антиоксидантов в составе сиропов должно быть строго обосновано с учетом их безопасности и целесообразности. Динатрия эдетат, несмотря на его эффективность как антиоксиданта и хелатирующего агента, требует осторожного подхода из-за потенциальной нефротоксичности. Аскорбиновая кислота, напротив, является безопасным и перспективным вариантом, и целесообразно ее более широкое применение.
Загустители
Большинство сиропов имеют вязкую консистенцию, что обеспечивает удобство дозирования. Зачастую роль загустителя выполняет сахароза, однако она обладает рядом недостатков, перечисленных выше, в связи с чем целесообразно рассмотреть полную или частичную ее замену на другие загустители [40]. Классификация и характеристики загустителей представлены на рисунке 2 и в таблице 4.

Рисунок подготовлен авторами / The figure is prepared by the authors
Рис. 2. Классификация загустителей по природе происхождения
Fig. 2. Classification of thickeners by origin
Загустители используются для регулирования вязкости состава, они могут маскировать неприятный вкус действующего вещества, усиливать сладкий вкус, продлевая нахождение ЛП в полости рта [40][41]. Некоторые загустители, в частности производные целлюлозы, могут повысить стабильность сиропов [40].
Одним из наиболее хорошо зарекомендовавших себя загустителей в сиропах (5,19% составов) является гиэтеллоза (гидроксиэтилцеллюлоза, ГЭЦ, natrosol) — водорастворимый эфир целлюлозы с случайно замещенными гидроксиэтильными группами в положениях 2, 3, 6 [42]. Она хорошо растворяется в холодной и горячей воде в отличие от других производных целлюлозы [40][42]. Неионогенная природа гиэтеллозы обеспечивает ее высокую стабильность в широком диапазоне pH (2–12) и совместимость со многими полимерами и ионами41 [40]. Чаще всего она используется в концентрациях от 0,1 до 0,15% и входит в состав сиропов от кашля, содержащих амброксол и экстракт плюща.
Кармеллоза натрия (карбоксиметилцеллюлоза натрия, E466) — анионное водорастворимое производное целлюлозы, в которой некоторые гидроксильные группы заменены карбоксильной группой [43]. В сиропах используется в качестве загустителя в концентрациях 0,1–1%42. Водные растворы стабильны при pH 3–11, а максимальная вязкость и стабильность проявляется при pH 7–943 [44]. Частота встречаемости — 1,42%.
Гипромеллоза (гидроксипропилметилцеллюлоза, ГПМЦ) представляет собой гидроксипропилметиловый эфир целлюлозы; характеризуется хорошей растворимостью в холодной воде с образованием коллоидного вязкого раствора [45]. ГПМЦ в сиропах применяется в качестве загустителя и стабилизатора в концентрациях 0,5–1,5% [46]. Водные растворы стабильны при pH 3–11 [44][46].
Производные целлюлозы признаны безопасными и широко используются при производстве многих ЛП [47]. Их безопасность объясняется тем, что они не гидролизуются и не попадают в кровоток [40]. Однако следует отметить, что производные целлюлозы в больших количествах обладают слабительным эффектом [47].
Ксантановая камедь (Е 415) (входит в 3,30% составов сиропов) — высокомолекулярный полисахарид, который вырабатывается грамотрицательными бактериями рода Xanthomonas campestris; устойчива к деградации и гидролизу, а также стабильна в средах с широким диапазоном pH и при высоких температурах. Ксантановая камедь имеет долгую историю применения в пищевой и фармацевтической промышленности и признана безопасной для взрослых и детей [48][49], используется в качестве загустителя, стабилизатора и эмульгатора в концентрациях от 0,1 до 0,15% [50].
Трагакантовая камедь (трагакант, Е413) встречается только в одном поливитаминном сиропе. Это высушенная на воздухе камедь, получаемая в основном из растений рода Astragalus, гетерогенный разветвленный анионный полисахарид с высокой молекулярной массой (840–850 кДа) [51]. Она также содержит небольшое количество целлюлозы, крахмала и белка, наиболее стабильна при pH от 4 до 844. Поскольку трагакантовая камедь представляет собой природный полисахарид, она считается немутагенной, неканцерогенной и нетератогенной [49], в редких случаях может вызывать реакции гиперчувствительности45.
Гуаровая камедь (гуаровый галактоманнан, Е412) — природная камедь, получаемая из измельченного эндосперма растения Cyamopsis Tetragonolobus46. Основа гуаровой камеди — водорастворимый полисахарид галактоманнан, который представляет собой смесь D-галактозы и D-маннозы [52]. Она практически нерастворима в органических растворителях, в горячей и холодной воде, быстро гидратируется при диспергировании и образует вязкий коллоидный раствор47 [52]. Гуаровая камедь обладает буферными свойствами, поэтому стабильна в широком диапазоне pH от 4 до 10,5, но чувствительна к длительному нагреванию. Она встречается только в одном муколитическом сиропе в концентрации 0,35%. Гуаровая камедь широко используется в пищевой промышленности и в фармации и считается безопасной. Чрезмерное потребление может вызывать метеоризм, диарею и тошноту48.
В состав двух сиропов (0,94%) входит натрия альгинат (Е401). Натрия альгинат является натриевой солью альгиновой кислоты — гетерополимера, образованного двумя остатками полиуроновых кислот (D-маннуроновой и L-гулуроновой) [53]. Он практически нерастворим в органических растворителях, медленно растворяется в воде с образованием вязкого коллоидного раствора, стабилен в широком диапазоне pH (от 4 до 10), при pH ниже 3 выпадает в осадок. Натрия альгинат признан безопасным веществом и широко применяется в пищевой, парфюмерно-косметической и фармацевтической промышленности49.
Выбор загустителей для сиропов должен основываться на их безопасности и функциональных свойствах. Использование производных целлюлозы следует ограничивать, чтобы избежать побочных эффектов, таких как слабительный эффект при больших концентрациях. В то же время природные полисахариды, такие как ксантановая камедь и натрия альгинат, обладают высокой безопасностью и стабильностью. Мы рекомендуем рассмотреть их более широкое применение в сиропах, особенно для детей, как альтернативу сахарозе.
Красители
Красители можно разделить на натуральные (природные) и синтетические, которые, в свою очередь, подразделяются на органические и неорганические (минеральные). При фармацевтической разработке нового ЛП цвет красителя подбирают в соответствии с запахом (ароматизатором) ЛП. В большинстве случаев концентрация красителя не превышает 0,001% [54]. Основные характеристики красителей представлены в таблице 4.
В состав сиропов входят натуральные и органические синтетические красители. Чаще всего в сиропах (7,55%) встречается желтый «Солнечный закат» (E110) — оранжевый полярный водорастворимый анионный моноазокраситель. Данный краситель может вызывать аллергические реакции, нарушение сна и изменение поведения у детей [55].
Понсо 4R (пунцовый 4R, E124) — красный водорастворимый анионный моноазокраситель. Недавние исследования на крысах показывают, что понсо 4R может вызывать нейрокогнитивные изменения [56], однако в целом исследований по безопасности недостаточно, чтобы сделать однозначный вывод о его безопасности.
Хинолиновый желтый — водорастворимый анионный краситель хинофталон желтого цвета. Он может вызывать аллергические реакции, в высоких дозах обладает генотоксическим эффектом, способен ингибировать холинэстеразу в эритроцитах и псевдохолинэстеразу плазмы крови [56].
Рибофлавин (Е101, витамин В2) является натуральным пищевым красителем ярко-желтого цвета.
Поскольку вопросы безопасности применения красителей остаются спорными, мы рекомендуем избегать добавления красителей в сиропы. Несмотря на широкое применение как натуральных, так и синтетических красителей, их потенциальные аллергические и токсические эффекты, особенно у детей, вызывают беспокойство.
ЗАКЛЮЧЕНИЕ
В ходе работы был проведен анализ вспомогательных веществ в сиропах, зарегистрированных в ГРЛС, с целью оценки их роли, безопасности и частоты использования.
Поскольку некоторые вещества, часто использующиеся при производстве лекарственных препаратов в качестве вспомогательных веществ, могут нести скрытые риски в отношении безопасности ЛП, особенно для детей, производителям необходимо обеспечить более ответственный подход к введению ВВ в состав ЛП. Избыточное использование подсластителей, консервантов или растворителей может повлиять на здоровье в долгосрочной перспективе. На основе выявленных данных следует пересмотреть существующие подходы к выбору вспомогательных веществ в сиропах, чтобы минимизировать потенциальные риски и повысить безопасность ЛП.
Полученные данные могут использоваться для формирования научно обоснованных рекомендаций, которые будут полезны медицинским работникам при назначении сиропов, фармацевтическим специалистам при консультировании и разработчикам ЛП для оптимизации выбора вспомогательных веществ при разработке.
Вклад авторов. Все авторы подтверждают соответствие своего авторства критериям ICMJE. Наибольший вклад распределен следующим образом: Я.С. Новиков — анализ инструкций по применению сиропов, зарегистрированных в ГРЛС, написание исходного текста рукописи, формулировка выводов, составление списка литературы; С.Н. Егорова — концепция работы, участие в написании текста рукописи и утверждение окончательной версии для публикации; В.В. Косенко — утверждение рукописи к публикации; Н.Д. Бунятян — участие в написании и редактировании текста рукописи; В.А. Евтеев — работа с источниками литературы.
Authors’ contributions. All the authors confirm that they meet the ICMJE criteria for authorship. The most significant contributions were as follows. Yaroslav S. Novikov analysed summaries of product characteristics for syrups registered in the Russian State Register of Medicines, drafted the original text of the manuscript, formulated the conclusions, and compiled the reference list. Svetlana N. Egorova conceptualised the study, drafted the manuscript, and approved its final version for publication. Valentina V. Kosenko approved the final version of the manuscript for publication. Natalya D. Bunyatyan drafted and edited the manuscript. Vladimir A. Evteev worked with literature.
1. 2017 European Commission report on the paediatric regulation.
2. ОФС.1.4.1.0012 Сиропы. Государственная фармакопея Российской Федерации. XV изд. М.; 2023.
3. Государственный реестр лекарственных средств.
4. Под приемлемостью сиропа следует понимать органолептические свойства (вкус, запах и цвет), повышающие приверженность (комплаентность) детей к лечению.
5. Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA).
6. SCOGS (Select Committee on GRAS Substances).
7. EMA/CHMP/704195/2013 Propylene glycol used as an excipient. Report published in support of the ‘Questions and answers on propylene glycol used as an excipient in medicinal products for human use’. EMA; 2013.
EMA/CHMP/SWP/272921/2012 Reflection paper on the use of methyl- and propylparaben as excipients in human medicinal products for oral use. EMA; 2015.
EMA/CHMP/272866/2013 Benzyl alcohol and benzoic acid group used as excipients. Report published in support of the ‘Questions and answers on benzyl alcohol used as an excipient in medicinal products for human use’ (EMA/CHMP/508188/2013) and the ‘Questions and answers on benzoic acid and benzoates used as excipients in medicinal products for human use’ (EMA/CHMP/508189/2013). EMA; 2017.
8. ADI — максимальное количество вещества, которое можно принимать внутрь ежедневно в течение жизни без заметного риска для здоровья, мг/кг массы тела в сутки.
9 .Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA).
10. SCOGS (Select Committee on GRAS Substances).
11. Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017.
12. Там же.
13. Государственный реестр лекарственных средств.
14. Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA).
15. SCOGS (Select Committee on GRAS Substances).
16. Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA).
17. Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017.
18. EMA/CHMP/SWP/272921/2012 Reflection paper on the use of methyl- and propylparaben as excipients in human medicinal products for oral use. EMA; 2015.
19. Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017.
20. EMA/CHMP/SWP/272921/2012 Reflection paper on the use of methyl- and propylparaben as excipients in human medicinal products for oral use. EMA; 2015.
21. Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA).
22. Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017.
23. Там же.
24. Государственный реестр лекарственных средств.
25. Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA).
26. SCOGS (Select Committee on GRAS Substances).
27. Там же.
28. EMA/CHMP/272866/2013 Benzyl alcohol and benzoic acid group used as excipients. Report published in support of the ‘Questions and answers on benzyl alcohol used as an excipient in medicinal products for human use’ (EMA/CHMP/508188/2013) and the ‘Questions and answers on benzoic acid and benzoates used as excipients in medicinal products for human use’ (EMA/CHMP/508189/2013). EMA; 2017.
29. Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017.
30. Там же.
31. Там же.
32. Там же.
33. Там же.
34. Там же.
35. EMA/CHMP/334655/2013 Propylene glycol used as an excipient. Report published in support of the ‘Questions and answers on propylene glycol used as an excipient in medicinal products for human use’ (EMA/CHMP/704195/2013). EMA; 2017.
36. Там же.
37. Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017.
38. Государственный реестр лекарственных средств.
39. Evaluations of the Joint FAO/WHO Expert Committee on Food Additives (JECFA).
40. SCOGS (Select Committee on GRAS Substances).
41. Sheskey PJ, Cook WG, Cable CG, eds. Handbook of pharmaceutical excipients. 8th ed. Washington, DC: Pharmaceutical Press; 2017.
42. Там же.
43. Там же.
44. Там же.
45. Там же.
46. Там же.
47. Там же.
48. Там же.
49. Там же.
Список литературы
1. Petkova V, Georgieva D, Dimitrov M, Nikolova I. Off-label prescribing in pediatric population — literature review for 2012–2022. Pharmaceutics. 2023;15(12):2652. https://doi.org/10.3390/pharmaceutics15122652
2. Malkawi WA, AlRafayah E, AlHazabreh M, AbuLaila S, Al-Ghananeem AM. Formulation challenges and strategies to develop pediatric dosage forms. Children. 2022;9(4):488. https://doi.org/10.3390/children9040488
3. Rusz C-M, Ősz B-E, Jîtcă G, Miklos A, Bătrînu M-G, Imre S. Off-label medication: From a simple concept to complex practical aspects. Int J Environ Res Public Health. 2021;18(19):10447. https://doi.org/10.3390/ijerph181910447
4. Moreira M, Sarraguça M. How can oral paediatric formulations be improved? A challenge for the XXI century. Int J Pharm. 2020;590:119905. https://doi.org/10.1016/j.ijpharm.2020.119905
5. Meyers RS. The past, present, and future of oral dosage forms for children. J Pediatr Pharmacol Ther. 2024;29(1):22–31. https://doi.org/10.5863/1551-6776-29.1.22
6. Saito J, Agrawal A, Patravale V, Pandya A, Orubu S, Zhao M, et al. The current states, challenges, ongoing efforts, and future perspectives of pharmaceutical excipients in pediatric patients in each country and region. Children (Basel). 2022;9(4):453. https://doi.org/10.3390/children9040453
7. Ким МЕ, Степанова ЭФ, Евсеева СБ. Сиропы: состав, технология, современное состояние исследований (обзор литературы). Фармация и фармакология. 2014;2(3):7–14. https://doi.org/10.19163/2307-9266-2014-2-3(4)-7-14
8. Meyers RS, Thackray J, Matson KL, McPherson C, Lubsch L, Hellinga RC, Hoff DS. Key potentially inappropriate drugs in pediatrics: The KIDs list. J Pediatr Pharmacol Ther. 2020; 25(3):175–91. https://doi.org/10.5863/1551-6776-25.3.175
9. Al Humaid J. Sweetener content and cariogenic potential of pediatric oral medications: A literature review. Int J Health Sci (Qassim). 2018;12(3):75–82. PMCID: PMC5969777
10. Wee M, Tan V, Forde C. A comparison of psychophysical dose-response behaviour across 16 sweeteners. Nutrients. 2018;10(11):1632. https://doi.org/10.3390/nu10111632
11. Cavagnari BM. Non-caloric sweeteners and body weight. Medicina (Buenos Aires). 2019;79(2):115–22. PMID: 31048277
12. Iizuka K. Is the use of artificial sweeteners beneficial for patients with diabetes mellitus? The advantages and disadvantages of artificial sweeteners. Nutrients. 2022;14(21):4446. https://doi.org/10.3390/nu14214446
13. Dulal MM, Islam MK, Chowdhury AA, Chowdhury JA. Prevention of cap-locking of syrup product by treating the manufacturing process of sugar syrup with citric acid monohydrate. Bangladesh Pharm J. 2016;19(2):190–6. https://doi.org/10.3329/bpj.v19i2.29279
14. White JR Jr. Sugar. Clin Diabetes. 2018;36(1):74–6. https://doi.org/10.2337/cd17-0084
15. Belayneh A, Tadese E, Molla F. Safety and biopharmaceutical challenges of excipients in off-label pediatric formulations. Int J Gen Med. 2020;13:1051–66. https://doi.org/10.2147/IJGM.S280330
16. Rouaz K, Chiclana-Rodríguez B, Nardi-Ricart A, Sune-Pou M, Mercade-Frutos D, Sune-Negre JM, et al. Excipients in the paediatric population: A review. Pharmaceutics. 2021;13(3):387. https://doi.org/10.3390/pharmaceutics13030387
17. Tan VWK, Wee MSM, Tomic O, Forde CG. Temporal sweetness and side tastes profiles of 16 sweeteners using temporal check-all-that-apply (TCATA). Food Res Int. 2019;121:39–47. https://doi.org/10.1016/j.foodres.2019.03.019
18. Grembecka M. Sugar alcohols — their role in the modern world of sweeteners: A review. Eur Food Res Technol. 2015;241:1–14. https://doi.org/10.1007/s00217-015-2437-7
19. Radeloff MA, Beck RHF. Polyols — more than sweeteners. Sugar Industry/Zuckerindustrie. 2013;138(4):226–34. https://doi.org/10.36961/si14095
20. Zhang W, Chen J, Chen Q, Wu H, Mu W. Sugar alcohols derived from lactose: Lactitol, galactitol, and sorbitol. Appl Microbiol Biotechnol. 2020;104(22):9487–95. https://doi.org/10.1007/s00253-020-10929-w
21. Bauditz J, Norman K, Biering H, Lochs H, Pirlich M. Severe weight loss caused by chewing gum. BMJ. 2008;336(7635):96–7. https://doi.org/10.1136/bmj.39280.657350.BE
22. Razzak Mahmood AA, Al-Juboori SB. A review: Saccharin discovery, synthesis, and applications. Ibn AL-Haitham J Pure Appl Sci. 2020;33(2):43–61. https://doi.org/10.30526/33.2.2442
23. More TA, Sheikh Z, Ali A. Artificial sweeteners and their health implications: A review. Biosci Biotech Res Asia. 2021;18(2). https://doi.org/10.13005/bbra/2910
24. Chattopadhyay S, Raychaudhuri U, Chakraborty R. Artificial sweeteners — a review. J Food Sci Technol. 2014;51(4):611–21. https://doi.org/10.1007/s13197-011-0571-1
25. Saad A. A review on potential toxicity of artificial sweeteners vs safety of stevia: A natural bio-sweetener. J Biol Agric Health Care. 2014;(4):137–47.
26. Magnuson BA, Roberts A, Nestmann ER. Critical review of the current literature on the safety of sucralose. Food Chem Toxicol. 2017;106(Pt A):324–55. https://doi.org/10.1016/j.fct.2017.05.047
27. Shaher SAA, Mihailescu DF, Amuzescu B. Aspartame safety as a food sweetener and related health hazards. Nutrients. 2023;15(16):3627. https://doi.org/10.3390/nu15163627
28. Petric Z, Ružić J, Žuntar I. The controversies of parabens — an overview nowadays. Acta Pharm. 2021;71(1):17–32. https://doi.org/10.2478/acph-2021-0001
29. Alaba P, Cañete E, Pantalan B, Taguba J, Yu L, Faller E. Toxic effects of paraben and its relevance in cosmetics: A review. Int J Res. 2022;3(5):3425–66.
30. Lincho J, Martins RC, Gomes J. Paraben compounds — Part I: An overview of their characteristics, detection, and impacts. Appl Sci. 2021;11(5):2307. https://doi.org/10.3390/app11052307
31. Walczak-Nowicka ŁJ, Herbet M. Sodium benzoate — harmfulness and potential use in therapies for disorders related to the nervous system: A review. Nutrients. 2022;14(7):1497. https://doi.org/10.3390/nu14071497
32. Raharjo S. Toxicological aspects of sorbates: A review. agriTECH. 2017;14(3):35–41. https://doi.org/10.22146/agritech.19294
33. Chilbule A, Singh R, Mann B, Arora S, Sharma R, Singh Rao P. Development and validation of an analytical method for determination of bronopol and kathon preservative in milk. J Food Sci Technol. 2019;56(6):3170–6. https://doi.org/10.1007/s13197-019-03807-5
34. Becker LC, Bergfeld WF, Belsito DV, Hill RA, Klaassen CD, Liebler DC, et al. Safety assessment of glycerin as used in cosmetics. Int J Toxicol. 2019;38(3_suppl):6S–22S. https://doi.org/10.1177/1091581819883820
35. Eccles R, Mallefet P. Soothing properties of glycerol in cough syrups for acute cough due to common cold. Pharmacy (Basel). 2017;5(1):4. https://doi.org/10.3390/pharmacy5010004
36. Marek E, Kraft WK. Ethanol pharmacokinetics in neonates and infants. Curr Ther Res. 2014;76:90–7. https://doi.org/10.1016/j.curtheres.2014.09.002
37. Zuccotti GV, Fabiano V. Safety issues with ethanol as an excipient in drugs intended for pediatric use. Expert Opin Drug Saf. 2011;10(4):499–502. https://doi.org/10.1517/14740338.2011.565328
38. Mohammadi Z, Shalavi S, Jafarzadeh H. Ethylenediaminetetraacetic acid in endodontics. Eur J Dent. 2013;7(Suppl 1):S135–S142. https://doi.org/10.4103/1305-7456.119091
39. Lanigan RS, Yamarik TA. Final report on the safety assessment of EDTA, calcium disodium EDTA, diammonium EDTA, dipotassium EDTA, disodium EDTA, TEA-EDTA, tetrasodium EDTA, tripotassium EDTA, trisodium EDTA, HEDTA, and trisodium HEDTA. Int J Toxicol. 2002;21 Suppl 2:95–142. https://doi.org/10.1080/10915810290096522
40. Jujare VK, Dantuluri A, Liu Y, Durig T. Hydroxyethylcellulose as a versatile viscosity modifier in the development of sugar-free, elegant oral liquid formulations. Int J Curr Res Chem Pharm Sci. 2023;10:1–23. https://doi.org/10.22192/ijcrcps.2023.10.04.001
41. Eccles R. What is the role of over 100 excipients in over-the-counter (OTC) cough medicines? Lung. 2020;198(5):727–34. https://doi.org/10.1007/s00408-020-00390-x
42. Arai K, Shikata T. Hydration/dehydration behavior of hydroxyethyl cellulose ether in aqueous solution. Molecules. 2020; 25(20):4726. https://doi.org/10.3390/molecules25204726
43. Rahman MS, Hasan MS, Nitai AS, Nam S, Karmakar AK, Ahsan MS, et al. Recent developments of carboxymethyl cellulose. Polymers (Basel). 2021;13(8):1345. https://doi.org/10.3390/polym13081345
44. Zarmpi P, Flanagan T, Meehan E, Mann J, Fotaki N. Biopharmaceutical understanding of excipient variability on drug apparent solubility based on drug physicochemical properties: Case study — hypromellose (HPMC). AAPS J. 2020;22(2):49. https://doi.org/10.1208/s12248-019-0411-1
45. Kruk K, Szekalska M, Basa A, Winnicka K. The impact of hypromellose on pharmaceutical properties of alginate microparticles as novel drug carriers for posaconazole. Int J Mol Sci. 2023;24(13):10793. https://doi.org/10.3390/ijms241310793
46. Binisha K, Remya SB, Prasobh GR, Jasbin Nisha S, Soorya S. A review on hypromellose as pharmaceutical excipient for oromucosal drug delivery. Int J Pharm Pharm Res. 2023;27(2):289–303.
47. Final report on the safety assessment of hydroxyethylcellulose, hydroxypropylcellulose, methylcellulose, hydroxypropyl methylcellulose, and cellulose gum. J Am Coll Toxicol. 1986;5(3):1–59. https://doi.org/10.3109/10915818609141925
48. Mortensen A, Aguilar F, Crebelli R, Di Domenico A, Frutos MJ, Galtier P, et al. Re-evaluation of xanthan gum (E 415) as a food additive. EFSA J. 2017;15(7):e04909. https://doi.org/10.2903/j.efsa.2017.4909
49. Cortes H, Caballero-Florán IH, Mendoza-Muñoz N, Escutia-Guadarrama L, Figueroa-González G, Reyes-Hernández OD, et al. Xanthan gum in drug release. Cell Mol Biol (Noisy-le-Grand). 2020;66(4):199–207. PMID: 32583796
50. Furtado I, Sydney E, Rodrigues S, Sydney A. Xanthan gum: Applications, challenges, and advantages of this asset of biotechnological origin. Biotechnol Res Innov. 2022;6:e202204. https://doi.org/10.4322/biori.202205
51. Patil N. Tragacanth gum-based hydrogels for drug delivery and tissue engineering applications. Front Mater. 2024;11. https://doi.org/10.3389/fmats.2024.1296399
52. Tripathy S, Das M. Guar gum: Present status and applications. J Pharm Sci Innov. 2013;2(4):24–8. https://doi.org/10.7897/2277-4572.02447
53. Abka-Khajouei R, Tounsi L, Shahabi N, Patel AK, Abdelkafi S, Michaud P. Structures, properties and applications of alginates. Mar Drugs. 2022;20(6):364. https://doi.org/10.3390/md20060364
54. Biswal PK, Mishra MK, Bhadouriya AS, Yadav VK. An updated review on colorants as the pharmaceutical excipients. Int J Pharm Chem Biol Sci. 2015;5(4):1004–17.
55. Barciela P, Perez-Vazquez A, Prieto MA. Azo dyes in the food industry: Features, classification, toxicity, alternatives, and regulation. Food Chem Toxicol. 2023;178:113935. https://doi.org/10.1016/j.fct.2023.113935
56. Amchova P, Kotolova H, Ruda-Kucerova J. Health safety issues of synthetic food colorants. Regul Toxicol Pharmacol. 2015;73(3):914–22. https://doi.org/10.1016/j.yrtph.2015.09.026
Об авторах
В. В. КосенкоРоссия
Косенко Валентина Владимировна - канд. фарм. наук.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Я. С. Новиков
Россия
Новиков Ярослав Сергеевич
Ул. Бутлерова, д. 49, Казань, 420012
С. Н. Егорова
Россия
Егорова Светлана Николаевна - д-р фарм. наук, профессор.
Ул. Бутлерова, д. 49, Казань, 420012
В. А. Евтеев
Россия
Евтеев Владимир Александрович
Петровский б-р, д. 8, стр. 2, Москва, 127051
Н. Д. Бунятян
Россия
Бунятян Наталья Дмитриевна - д-р фарм. наук, профессор.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Дополнительные файлы
Рецензия
Для цитирования:
Косенко В.В., Новиков Я.С., Егорова С.Н., Евтеев В.А., Бунятян Н.Д. Роль и безопасность вспомогательных веществ в лекарственной форме «сиропы»: обзор. Регуляторные исследования и экспертиза лекарственных средств. 2025;15(2):190-205. https://doi.org/10.30895/1991-2919-2025-15-2-190-205
For citation:
Kosenko V.V., Novikov Ya.S., Egorova S.N., Evteev V.A., Bunyatyan N.D. Role and Safety of Excipients in Syrups (Review). Regulatory Research and Medicine Evaluation. 2025;15(2):190-205. (In Russ.) https://doi.org/10.30895/1991-2919-2025-15-2-190-205



































