Перейти к:
Элементы стратегического планирования патентной охраны фармацевтических разработок
https://doi.org/10.30895/1991-2919-2024-14-5-513-520
Резюме
ВВЕДЕНИЕ. Коммерческий успех инновационных разработок в медицине и фармации напрямую зависит от стратегического планирования патентной охраны, основными элементами которого являются режим патентной правовой охраны, объект изобретения, последовательность получения охранных документов.
ЦЕЛЬ. Анализ особенностей стратегического планирования патентной охраны фармацевтической разработки.
МАТЕРИАЛЫ И МЕТОДЫ. В исследовании применялись аналитический и сравнительный методы исследования патентной информации. Для подготовки статистических данных использовались патентные базы данных: поисковая платформа Роспатента и Questel.
РЕЗУЛЬТАТЫ. В Российской Федерации количество патентов на изобретения, относящихся к способам лечения и диагностики, превалирует над патентами, относящимися к фармацевтическому продукту. Наиболее рациональным способом охраны права интеллектуальной собственности в фармацевтической отрасли является поэтапное получение разного вида охранных документов в рамках одного проекта на различные объекты патентного права: изобретения, полезные модели, промышленные образцы. При построении стратегии патентной охраны фармацевтической разработки следует учитывать: выбор режима патентной охраны (охрана разработки одновременно с использованием патентов на изобретения, полезные модели и промышленные образцы); корректное определение объекта патентования (получение патента на «продукт» (вещество)); поэтапное получение разного вида охранных документов и наращивание их.
ВЫВОДЫ. Представленная стратегия позволяет в наибольшей степени охватить все возможные варианты охраны прав на разработку и предупредить нарушения, а также удлинить срок правовой охраны разработки.
Ключевые слова
Для цитирования:
Аникеева М.Ю., Горбунова Ю.А., Пикина Н.А. Элементы стратегического планирования патентной охраны фармацевтических разработок. Регуляторные исследования и экспертиза лекарственных средств. 2024;14(5):513-520. https://doi.org/10.30895/1991-2919-2024-14-5-513-520
For citation:
Anikeeva M.Yu., Gorbunova Yu.A., Pikina N.A. Elements of Strategic Planning of Patent Protection for Pharmaceutical Inventions. Regulatory Research and Medicine Evaluation. 2024;14(5):513-520. (In Russ.) https://doi.org/10.30895/1991-2919-2024-14-5-513-520
ВВЕДЕНИЕ
В свете последних вызовов, с которыми столкнулась экономика России, в частности в сфере медицины и здравоохранения, решение задач импортозамещения будет содействовать обеспечению населения России качественными и эффективными лекарственными средствами, а также медицинскими изделиями, отвечающими требованиям фармацевтической и биологической безопасности. Особую коммерческую ценность при решении этих задач представляют разрабатываемые новые продукты и технологии их получения. В связи с этим крайне важно обеспечить их правовую охрану [1].
Обеспечение правовой охраны является одним из ключевых аспектов в выстраивании связей между исследователями-разработчиками и индустриальными партнерами, тем самым оказывая значительное влияние на экономику государства.
Цель работы — анализ особенностей стратегического планирования патентной охраны фармацевтической разработки.
МАТЕРИАЛЫ И МЕТОДЫ
Объектом исследования являлись отношения в области патентования в фармацевтической отрасли Российской Федерации. В исследовании применяли методы: статистический, сравнительный, классификации и анализа — с целью выявления наиболее значимых групп технологий, тенденций и стратегий патентования на территории Российской Федерации.
Законодательство (ст. 1225 Гражданского кодекса Российской Федерации (ГК РФ)) предлагает на выбор разные формы охраны разработок в сфере медицины и здравоохранения, в том числе в виде объектов патентных прав (изобретение, полезная модель, промышленный образец). В качестве изобретения охраняется техническое решение в любой области, относящееся к продукту (в частности, устройству, веществу, штамму микроорганизма, культуре клеток растений или животных) или способу (процессу осуществления действий над материальным объектом с помощью материальных средств), в том числе к применению продукта или способа по определенному назначению (п. 1 ст. 1350 ГК РФ). В качестве полезной модели охраняется техническое решение, относящее к устройству (п. 1 ст. 1351 ГК РФ), а в качестве промышленного образца охраняется решение внешнего вида изделия промышленного или кустарно-ремесленного производства (п. 1 ст. 1352 ГК РФ).
В ходе исследования проведен анализ патентных портфелей медицинских организаций на территории Российской Федерации. Схема анализа состоит из трех основных этапов [2]:
1) формирование поискового запроса, получение охранных документов, осуществление выгрузки из патентных баз данных;
2) структуризация полученных патентных данных;
3) визуальный вывод патентных данных (графическое представление).
Анализ проведен с использованием баз данных: поисковая платформа Роспатента1, информационно-поисковая система ФГБУ «Федеральный институт промышленной собственности»2, в качестве основной поисковой базы был выбран ORBIT INTELLIGENCE (Questel)3.
Патентная информация имеет преимущества по сравнению с другими видами научно-технических сведений, так как патент является источником информации, включающим сведения об объеме прав патентообладателей [3]. Методика построения патентного исследования соответствует требованиям, приведенным в ГОСТ 15.011-2024 «Интеллектуальная собственность. Патентные исследования. Содержание и порядок проведения».
Для анализа был выбран временной период — последние 20 лет, данное решение было связано с периодом охраны исключительных прав на изобретения. Для формирования поискового запроса были использованы фильтры ORBIT INTELLIGENCE (Questel): технологические области (медицина, фармацевтика, биотехнологии) и правообладатель (***Минздрава России).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Динамика патентования в фармацевтической отрасли в Российской Федерации. Ежегодно в области медицины, фармацевтики и биотехнологий в России резидентами подается 4000–4500 заявок на изобретения4 (рис. 1), что свидетельствует о значимости процедуры получения правовой охраны для организаций, занимающихся медицинскими и фармацевтическими разработками. По данным исследования [4] за период 2001–2023 гг. подведомственными учреждениями Минздрава России (далее — учреждения) получено около 30000 патентов Российской Федерации на изобретение (около трети от всего количества). По состоянию на 1 апреля 2024 г. поддерживаются в силе около 4800 патентов на изобретение, права на которые принадлежат 91 учреждению.
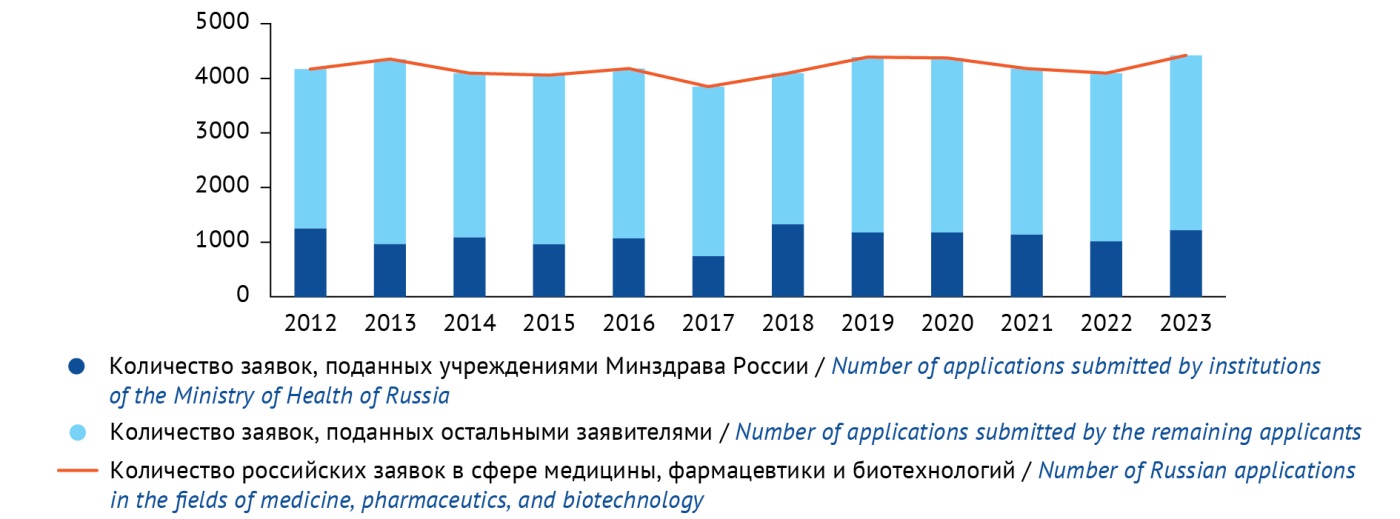
Рисунок подготовлен авторами по данным ORBIT INTELLIGENCE (Questel) / The figure is prepared by the authors using data from ORBIT INTELLIGENCE (Questel)
Рис. 1. Динамика подачи заявок на изобретения за 2012–2023 гг.
Fig. 1. Distribution of invention applications submitted in 2012–2023
Для дальнейшего анализа все действующие патенты учреждений были сгруппированы в соответствии с верхнеуровневой классификацией на лекарственные средства, медицинские изделия, медицинские технологии. К лекарственным средствам были отнесены химические соединения, белки, антитела, фармацевтические композиции, продукты биотехнологий (штаммы микроорганизмов, культуры клеток растений или животных и т.д.), способы получения соединений, фармацевтических субстанций. К медицинским изделиям были отнесены устройства и аппараты. К медицинским технологиям — способы диагностики, прогнозирования, лечения и др. Первые две категории можно отнести к так называемым «продуктовым» патентам. На территории Российской Федерации прослеживается тенденция превалирования патентов, относящихся к медицинским технологиям, а именно к способам диагностики и лечения заболевания (73% от общего количества действующих патентов), над «продуктовым» патентами, в которые входят лекарственные средства (19%), медицинские изделия (8%).
В случае получения патента в рамках разработки лекарственного средства исключительно на медицинскую технологию при отсутствии патента на продукт (например, структурная формула химического соединения, входящая в состав лекарственного средства) существует ряд рисков, с которыми может столкнуться правообладатель, а именно:
- трудность установления факта незаконного использования медицинской технологии, поскольку подобные технологии являются закрытыми производственными процессами;
- получение патента третьим лицом на аналогичную технологию;
- сложность коммерциализации технического решения, охарактеризованного исключительно в качестве способа, так как на рынке более востребованы «продуктовые» патенты.
Для успешного выведения лекарственного средства на рынок целесообразно использовать стратегию получения правовой охраны в форме последовательного получения разного вида охранных документов в рамках одного проекта на различные объекты интеллектуальной собственности.
Режим патентной правовой охраны. Согласно нормам российского законодательства объектами патентного права являются изобретение, полезная модель, промышленный образец (табл. 1). Получение патента на изобретение является наиболее часто применяемым видом патентной охраны фармацевтических разработок. Патент удостоверяет исключительные права (ст. 1354 ГК РФ) на ограниченный промежуток времени и на конкретной территории. Для получения патента на изобретение необходимо подтвердить, что разработка является новой, имеет изобретательский уровень и может быть промышленно применима (ст. 1350 ГК РФ).
Таблица 1. Характеристика объектов патентных прав
Table 1. Characteristics of objects of patent protection
Параметры Parameters | Вид объекта патентных прав Types of objects of patent protection | ||
Изобретение Invention | Полезная модель Utility model | Промышленный образец Industrial design | |
Условия патентоспособности Patentability requirements | Новизна; изобретательский уровень; промышленная применимость Novelty; non-obviousness; industrial applicability | Новизна; промышленная применимость Novelty; industrial applicability | Новизна; оригинальность Novelty; originality |
Предмет патента Object of protection | Техническое решение: продукт (вещество, химическая формула); способ; применение Technical solution: product (substance, chemical formula); method; application | Устройство Apparatus | Внешний вид изделия Product appearance |
Возможность объединения группы объектов в одной заявке Possibility of combining several objects in one application | Допустимо Acceptable | Недопустимо Inacceptable | Допустимо Acceptable |
Объем правовой охраны Scope of legal protection | Независимый пункт формулы Independent claim | Независимый пункт формулы Independent claim | Изображение внешнего вида изделия (словесные элементы не охраняются в качестве промышленного образца) Depiction of the appearance of a product (industrial designs do not protect verbal elements) |
Сроки действия исключительных прав Patent protection period | 20 лет 20 years | 10 лет 10 years | 5 лет 5 years |
Возможность продления правовой охраны Possibility of patent extension | До 5 лет Up to 5 years | Не предусмотрено Not applicable | Каждые 5 лет на срок до 5 лет (в целом не более чем на 25 лет) Up to 5 years every 5 years (no more than 25 years in total) |
Периодичность оплаты патентной пошлины Renewal fee frequency | Каждые 5 лет Every 5 years | ||
Возможность восстановления патента Possibility of patent restoration | В течение 3 лет Within 3 years | ||
Таблица составлена авторами / The table is prepared by the authors
Охрана разработки в рамках одного проекта одновременно в качестве изобретения, полезной модели и промышленного образца позволит обеспечить комплексную охрану интеллектуальной собственности. Этот подход дает возможность максимально закрепить за организацией-разработчиком исключительные права на его использование и коммерциализацию с учетом всех характеристик и аспектов разработки: функциональность, новизну, а также эстетическую ценность. Это позволяет создать многослойную систему защиты, где каждая форма охраны дополняет и усиливает другую.
Объект изобретения. Эффективной стратегией охраны интеллектуальной собственности при разработке лекарственного средства является получение правовой охраны на «продукт». К продуктам относятся вещества (химические соединения (в частности, нуклеиновые кислоты и белки), композиции (составы, смеси), продукты ядерного превращения), штаммы микроорганизмов, культуры клеток растений или животных, генетические и белковые конструкции, устройства5.
Наибольший объем правовой охраны среди объектов патентных прав, являющихся веществом, имеет патент на несколько химических соединений (вариантов), охарактеризованных структурной формулой Маркуша. Изначально название «группа Маркуша» было присвоено заявкам, в которых перечислялись химические фрагменты, «выбранные из группы, состоящей из списка альтернатив». Впоследствии термин «структура Маркуша» стал обозначать любую химическую структуру, которая содержит необходимую субструктуру и одну или несколько переменных химических групп [4]. Посредством формулы Маркуша, формат которой признан в патентном праве многих стран, можно охватить весь объем альтернатив в одной формуле изобретения6.
Особенностью формулы Маркуша является то, что в формуле изобретения указывается не конкретное соединение, а общая структурная формула группы химических соединений со схожей структурой, различающихся заместителями и (или) радикалами. В материалах заявки, содержащей формулу Маркуша, должны быть приведены примеры, подтверждающие возможность получения соединений заявленной структуры с разными по химической природе функциональными группами, а также доказательства возможности использования их по предполагаемому назначению7. Данная стратегия патентования позволит патентообладателю получить правовую охрану на соединения (варианты), которые в том числе не раскрыты в патенте. Следовательно, без согласия патентообладателя становится невозможным использование любого химического соединения, охраняемого формулой Маркуша, даже в случае, если данное соединение не входит в состав лекарственного средства. С другой стороны, патентообладатель получает возможность в будущем исследовать свойства охраняемых продуктов, и в дальнейшем перед патентообладателем открываются перспективы применения таких продуктов в новых смежных областях, а также возможность расширения перечня охраняемых продуктов без дополнительной процедуры патентования.
В стратегию патентной охраны наряду с изобретениями, описанными формулами Маркуша, включают селективные изобретения совместно с изобретениями, описанными посредством формулы Маркуша. Селективное изобретение — это химическое соединение, подпадающее под общую структурную формулу группы известных соединений, но не описанное как специально полученное и исследованное и при этом проявляющее новые, неизвестные для этой группы свойства в качественном или количественном отношении8. Иными словами, в ходе проведения научных исследований может быть выявлено новое химическое соединение с определенными свойствами, структура которого соответствует заявленной ранее в формуле Маркуша, охраняемой действующим патентом. Если данное новое химическое соединение не указано как таковое и не описаны его характеристики, тогда возможно получение патента на селективное изобретение. При подготовке патентной заявки необходимо описать конкретную структуру нового химического соединения, а также указать новые, неизвестные ранее свойства в качественном и (или) количественном отношении.
При написании заявки на получение патента на изобретение в патентных формулах могут быть представлены объекты изобретения разного рода с характеристиками существенных признаков, выраженных в общем виде, которые позволяют охватить возможные варианты или модификации с перспективой совершенствования охраняемого объекта. Преимуществом такого метода являются низкие затраты на оплату патентных пошлин, так как в одном охранном документе представлены объекты разного рода.
Последовательность получения охранных документов. Построение патентной стратегии, посредством которой организация-разработчик поэтапно в рамках одной фармацевтической разработки получает правовую охрану на изобретения, позволяет наиболее широко охватить охрану возможных вариантов или модификаций фармацевтической разработки.
В рамках первого этапа построения такой стратегии следует получить правовую охрану на индивидуальную молекулу либо химическое соединение, охарактеризованное структурной формулой Маркуша. После этого возможно получение охранных документов на фармацевтические композиции (с целью получения лекарственного средства (ЛС1)), а также получение патента на комбинации (в состав которых будут входить ЛС1 и уже ранее известные лекарственные средства), при этом патентование возможно при подтверждении нового технического результата и (или) при достижении синергетического эффекта. Финальным этапом при патентовании «фармацевтических изобретений» является получение охранных документов на способы изготовления (получения) указанных композиций и комбинаций, способы диагностики заболеваний, а также на применение фармацевтических композиций и (или) комбинаций по определенному назначению.
Особое место при разработке патентной стратегии занимает определение вариантов охраны промежуточных продуктов фармацевтических разработок. Решение вопроса об утилизации и вторичном применении таких продуктов, а также отходов производства, включается в перечень первоочередных мероприятий при разработке процессов производства лекарственных средств. Охрана промежуточных продуктов фармацевтических разработок для правообладателей может оказать значительное влияние на развитие конкурентного преимущества компании. Использование промежуточных продуктов в совершенно иных сферах деятельности может привести к разработке новых технологий, которые предоставят компании преимущество на рынках, что поспособствует стимулированию инноваций. В рамках разработки стратегии охраны промежуточного продукта в качестве изобретения правовая охрана может быть предоставлена на структуру промежуточного продукта (например, структурную формулу химического соединения или структурные характеристики биотехнологического объекта), способ получения промежуточного продукта и его применение по определенному назначению.
Следующий этап в построении патентной стратегии в рамках одного проекта — получение охранных документов на другие объекты патентных прав.
Патент на полезную модель предоставляет охрану технического решения, относящегося к устройству (ст. 1351 ГК РФ). При рассмотрении фармацевтических разработок получение патента на полезную модель возможно, например, при патентовании устройства для очистки вещества от примесей либо разработке или доработке технологического устройства (отдельного его конструктивного элемента или производственной линии), они могут быть также запатентованы в качестве полезной модели.
Возможно получение патента на промышленный образец, который предоставляет охрану внешнего вида изделия промышленного или кустарно-ремесленного производства (ст. 1352 ГК РФ). Данным способом можно охранять: геометрические параметры или внешнее оформление лекарственной формы (а именно таблетки, капсулы), например цвет, рисунок, узор, нанесенный на оболочку; вид первичной упаковки лекарственного средства, например нестандартное решение внешнего вида, нанесенный узор и сочетание цветов; вид вторичной упаковки лекарственного средства, например нестандартное решение внешнего вида, нанесенный узор и сочетание цветов. Нестандартное решение внешнего вида объектов будет привлекать внимание покупателей и поэтому дает преимущество производителю на рынке.
ЗАКЛЮЧЕНИЕ
На основании анализа возможных форм патентной охраны разработок в сфере медицины и здравоохранения в соответствии с законодательством Российской Федерации определены элементы стратегического планирования получения патентной охраны фармацевтических разработок:
- правовая охрана фармацевтических разработок с использованием разных объектов интеллектуальной собственности. Такой подход позволит многократно снизить возможность нарушения исключительных прав. Охрана разработок в разных режимах позволяет всесторонне охватить аспекты фармацевтической разработки, а также в случае нарушения исключительных прав доказать факт нарушения будет легко;
- получение патента на изобретение на продукт, а именно вещество (химическое соединение). Наличие патента на химические соединения, охватывающие несколько вариантов структурной формулы (в формате формулы Маркуша), предоставляет уникальные возможности для разработчиков новых веществ;
- получение охранных документов не единовременно, а в течение длящегося периода. Это позволит продлить срок охраны разработок и дольше иметь коммерческие преимущества на рынке.
Следует также отметить, что отсутствие должного стратегического планирования получения правовой охраны влияет на степень привлекательности и возможность коммерциализации продукции. В случае отсутствия достаточной степени охраны объектов интеллектуальной собственности повышаются правовые, коммерческие и налоговые риски бизнес-процессов и потенциальные инвесторы и индустриальные партнеры будут в меньшей степени заинтересованы в сотрудничестве.
Вклад авторов. Все авторы подтверждают соответствие своего авторства критериям ICMJE. Наибольший вклад распределен следующим образом: Ю.А. Горбунова — концепция работы, написание текста рукописи, участие в формулировании заключения, утверждение окончательной версии рукописи для публикации; М.Ю. Аникеева — проведение аналитических исследований в сфере интеллектуальной собственности, работа с иллюстративным материалом, участие в формулировании заключения; Н.А. Пикина — работа с источниками литературы.
Authors’ contributions. All the authors confirm that they meet the ICMJE criteria for authorship. The most significant contributions were as follows. Yuliya A. Gorbunova conceptualised the study, drafted the manuscript, participated in drawing the conclusions, and approved the final version of the manuscript for publication. Marina Yu. Anikeeva conducted analytical research in the sphere of intellectual property, worked with the graphical material, and participated in drawing the conclusions. Nina A. Pikina worked with literature sources.
1. https://searchplatform.rospatent.gov.ru/
2. https://www.fips.ru/elektronnye-servisy/informatsionno-poiskovaya-sistema/
3. https://www.orbit.com
4. Там же.
5. Приказ Министерства экономического развития Российской Федерации от 21.02.2023 № 107 «О государственной регистрации изобретений» (вместе с «Правилами составления, подачи и рассмотрения документов, являющихся основанием для совершения юридически значимых действий по государственной регистрации изобретений», «Требованиями к документам заявки на выдачу патента на изобретение», «Порядком проведения информационного поиска в отношении заявленного изобретения при проведении экспертизы по существу по заявке на выдачу патента на изобретение и представления отчета о нем», «Порядком публикации отчета об информационном поиске в отношении заявленного изобретения»).
6. WIPO, Summary: further study on the sufficiency of disclosure (Part II), 16–20 October 2023. https://www.wipo.int/edocs/mdocs/scp/en/scp_35/scp_35_5_summ.pdf
7. Приказ Министерства экономического развития Российской Федерации от 21.02.2023 № 107 «О государственной регистрации изобретений» (вместе с «Правилами составления, подачи и рассмотрения документов, являющихся основанием для совершения юридически значимых действий по государственной регистрации изобретений», «Требованиями к документам заявки на выдачу патента на изобретение», «Порядком проведения информационного поиска в отношении заявленного изобретения при проведении экспертизы по существу по заявке на выдачу патента на изобретение и представления отчета о нем», «Порядком публикации отчета об информационном поиске в отношении заявленного изобретения»).
8. Там же.
Список литературы
1. Allred BB, Park WG. The influence of patent protection on firm innovation investment in manufacturing industries. J Int Manag. 2007;13(2):91–109. https://doi.org/10.1016/j.intman.2007.02.001
2. Lei L, Qi J, Zheng К. Patent analytics based on feature vector space model. IEEE Access. 2019;7:45705–15. https://doi.org/10.1109/ACCESS.2019.2909123
3. Abbas А, Zhang L, Khan SU. A literature review on the state-of-the-art in patent analysis. World Pat Inf. 2014;37:3–13. https://doi.org/10.1016/j.wpi.2013.12.006
4. Косенко ВВ, Беланов КЮ, Федорова ДИ, Попов НВ. Исследование патентных портфелей подведомственных организаций Минздрава России. Вестник ФИПС. 2024:3(1):74–82. EDN: HIISRA
Об авторах
М. Ю. АникееваРоссия
Аникеева Марина Юрьевна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Ю. А. Горбунова
Россия
Горбунова Юлия Александровна.
Петровский б-р, д. 8, стр. 2, Москва, 127051
Н. А. Пикина
Россия
Пикина Нина Александровна.
Бережковская наб., д. 30, корп. 1, Москва, Г-59, ГСП-3, 125993
Рецензия
Для цитирования:
Аникеева М.Ю., Горбунова Ю.А., Пикина Н.А. Элементы стратегического планирования патентной охраны фармацевтических разработок. Регуляторные исследования и экспертиза лекарственных средств. 2024;14(5):513-520. https://doi.org/10.30895/1991-2919-2024-14-5-513-520
For citation:
Anikeeva M.Yu., Gorbunova Yu.A., Pikina N.A. Elements of Strategic Planning of Patent Protection for Pharmaceutical Inventions. Regulatory Research and Medicine Evaluation. 2024;14(5):513-520. (In Russ.) https://doi.org/10.30895/1991-2919-2024-14-5-513-520



































