Перейти к:
Разработка методики количественного определения холина в каплях ушных на основе омелы белой листьев экстракта густого
https://doi.org/10.30895/1991-2919-2025-668
Резюме
ВВЕДЕНИЕ. Причиной разработки нового состава капель, обладающих церуменолитическим действием, на основе экстракта густого омелы белой листьев (Viscum album L.) явился неудовлетворенный спрос на препараты такого действия. Одним из обязательных этапов подготовки регистрационного досье на лекарственное средство является разработка методики количественного анализа основного действующего вещества (холина), содержащегося в омелы белой листьев экстракте густом.
ЦЕЛЬ. Разработка методики количественного определения с последующей валидацией холина в каплях ушных церуменолитического действия на основе Viscum album листьев экстракта густого.
МАТЕРИАЛЫ И МЕТОДЫ. Наличие азотистых оснований устанавливали методом бумажной хроматографии. В качестве неподвижной фазы использовали бумагу хроматографическую марки Munktell (класс FN7, размер 4×25 см). В качестве подвижной фазы применяли системы растворителей: н-бутанол — этанол — уксусная кислота — вода (8:2:1:3), н-бутанол — уксусная кислота — вода (4:1:5), уксусная кислота — вода (15:85); в качестве проявителя — пары йода. Спектрофотометрическое определение азотистых оснований проводили с использованием спектрофотометра СФ-102, длина волны 400±2 нм, в присутствии соли рейнеката аммония (соли Рейнеке). Валидацию методики количественного определения сложных эфиров холина проводили по показателям: специфичность, линейность, правильность, прецизионность.
РЕЗУЛЬТАТЫ. Разработана и валидирована методика количественного определения содержания сложных эфиров холина в пересчете на холин в ушных каплях церуменолитического действия на основе омелы белой листьев экстракта густого, основанная на спектрофотометрическом определении в присутствии соли Рейнеке. В анализируемых ушных каплях с использованием разработанной методики идентифицированы холин и его сложные эфиры: ацетилхолин, йодид ацетилхолина и бензоилхолин. Содержание сложных эфиров холина в пересчете на холин составило 0,710±0,018%.
ВЫВОДЫ. Разработанная методика количественного определения сложных эфиров холина, основанная на спектрофотометрическом определении в присутствии соли Рейнеке, может быть предложена для контроля качества капель ушных церуменолитического действия на основе омелы белой листьев экстракта густого.
Ключевые слова
Для цитирования:
Аджиахметова С.Л., Позднякова А.Е. Разработка методики количественного определения холина в каплях ушных на основе омелы белой листьев экстракта густого. Регуляторные исследования и экспертиза лекарственных средств. 2025;15(1):57-62. https://doi.org/10.30895/1991-2919-2025-668
For citation:
Adzhiakhmetova S.L., Pozdnyakova A.E. Development of an Analytical Procedure for the Quantitative Determination of Choline in Ear Drops Based on Viscum album Leaf Soft Extract. Regulatory Research and Medicine Evaluation. 2025;15(1):57-62. (In Russ.) https://doi.org/10.30895/1991-2919-2025-668
ВВЕДЕНИЕ
Ушная сера обеспечивает механическую и микробиологическую защиту эпителиального слоя наружного слухового прохода. При накоплении ушной серы вследствие нарушения естественного механизма самоочищения уха может образоваться серная пробка. Скопление ушной серы препятствует оценке состояния уха, а при патологическом процессе вызывает неприятные симптомы: шум в ушах, чувство распирания, боль, что в случае запущенного состояния приводит к потере слуха [1]. Чаще сталкиваются с такой проблемой около 10% детей и одна треть лиц пожилого возраста с когнитивными нарушениями [2].
Важными параметрами при определении стратегии лечения серных пробок являются: фармакоэкономические факторы, стоимость препаратов, количество необходимых медицинских вмешательств, приверженность к лечению, сопутствующие нежелательные явления (например, нейросенсорная тугоухость), скорость улучшения качества жизни [3]. Методы удаления серной пробки, как правило, включают ирригацию и ручное удаление с помощью специализированных инструментов, могут быть также использованы церуменолитики (вещества, размягчающие ушную серу) [4][5].
Неудовлетворенный спрос на лекарственные препараты церуменолитического действия явился причиной разработки нового состава на основе омелы белой листьев (Viscum album L.) экстракта густого [6][7]. Основным действующим веществом листьев V. album является холин, обладающий церуменолитическим действием [8], а его содержание зависит от фазы вегетации и составляет 2,9–5,1%. Представляется необходимым разработка валидированной методики количественного анализа по холину в каплях ушных на основе омелы белой листьев экстракта густого.
Цель работы — разработка методики количественного определения холина в каплях ушных церуменолитического действия на основе омелы белой листьев экстракта густого.
МАТЕРИАЛЫ И МЕТОДЫ
Объектом исследования являлись капли ушные церуменолитического действия на основе омелы белой листьев экстракта густого. Разработка состава и технологии производства ушных капель представлена в работе [6]. Состав ушных капель церуменолитического действия: омелы белой листьев экстракт густой 0,0250 г; гиалуронат натрия 0,2000 г; бензалкония хлорид 0,0075 г; вода очищенная до 25 мл. Состав модельной смеси: гиалуронат натрия 0,2000 г; бензалкония хлорид 0,0075 г; вода очищенная до 25 мл.
Качественное определение азотистых оснований. Наличие азотистых оснований устанавливали методом бумажной хроматографии, поскольку известны факторы удерживания холина и его сложных эфиров, что позволяет сравнивать полученные результаты с данными литературы, не прибегая к использованию в ходе анализа стандартных образцов [9][10]. Это упрощает воспроизведение процедуры и дает экономические преимущества перед другими методиками (возможность воспроизведения методики анализа в лабораториях с недостаточным оснащением).
В качестве неподвижной фазы использовалась бумага хроматографическая Munktell (класс FN7, размер 4×25 см). В качестве подвижной фазы применяли систему растворителей Аугустинсо и Грана: н-бутанол — этанол — уксусная кислота — вода (8:2:1:3)1. Также использовали системы элюентов: н-бутанол — уксусная кислота — вода (4:1:5), уксусная кислота — вода (15:85). В качестве проявителя выступали пары йода.
Для нанесения пробы использовали дозатор механический одноканальный варьируемого объема, 0,5–10 мкл (BIOHIT). Объем наносимой пробы исследуемых ушных капель — 10 мкл.
Количественное определение сложных эфиров холина. Одним из точных и высокоселективных методов среди известных инструментальных методов количественного определения является высокоэффективная жидкостная хроматография. Применение этого метода, однако, имеет ряд экономических ограничений, например необходимость использования нескольких стандартных образцов. В этой связи целесообразнее использовать более доступный с позиции себестоимости анализа метод, каким является спектрофотометрия. В основе методики количественного содержания азотистых оснований лежит определение оптической плотности окрашенных комплексов холина и его производных с рейнекатом аммония (солью Рейнеке) [11][12].
В мерную колбу вместимостью 50 мл взвешивали и помещали 25,0 мл исследуемых ушных капель, доводили объем раствора до метки водой очищенной (раствор А). 30,0 мл раствора А помещали в мерную колбу вместимостью 100 мл и прибавляли по каплям 2 М раствор кислоты хлористоводородной (35,0%, х.ч., OOO «Химпром-М») до pH 3 (по универсальному индикатору). Полученный раствор охлаждали до 0 ºС, прибавляли 45 мл раствора соли Рейнеке (95,0%, ч., OOO «ХимКрафт»), оставляли в холодильнике на 18 ч при температуре 8 ºС и доводили объем раствора до метки водой очищенной. Осадок отфильтровывали через стеклянный фильтр № 4 и промывали на ледяной бане н-бутанолом (99,7%, х.ч., OOO «Химпром-М») 3 раза порциями по 5 мл. Затем осадок на фильтре растворяли при этой же температуре в ацетоне (99%, х.ч., OOO «Химпром-М») и объем полученного фильтрата доводили в мерной колбе ацетоном до 10 мл.
Оптическую плотность полученного раствора измеряли не позднее чем через 5 мин на спектрофотометре СФ-102 с максимумом поглощения при длине волны 400±2 нм в кювете с толщиной слоя 10 мм. В качестве раствора сравнения использовали ацетон. Параллельно в тех же условиях измеряли оптическую плотность раствора стандартного образца (СО) холин-хлорида с солью Рейнеке.
Приготовление раствора стандартного образца холин-хлорида. Около 0,2 г (точная навеска) стандартного образца (СО) холин-хлорида помещали в мерную колбу вместимостью 25 мл, растворяли в 9 мл воды очищенной, прибавляли по каплям 2 М раствор кислоты хлористоводородной до pH 3 по универсальному индикатору. Полученный раствор охлаждали до 0 °С, прибавляли 15 мл раствора соли Рейнеке, оставляли в холодильнике на 18 ч и доводили объем раствора до метки водой очищенной. Осадок отделяли и при этой же температуре растворяли в минимальном объеме ацетона, затем доводили тем же растворителем до объема 10 мл. 3,0 мл полученного раствора переносили в мерную колбу вместимостью 10 мл и доводили объем раствора до метки тем же растворителем. Оптическую плотность раствора измеряли не позднее чем через 5 мин. Использовали СО холин-хлорида (98%, Sigma-Aldrich, кат. номер а6625).
Содержание холина в пересчете на холин-хлорид (X%, %) вычисляли по формуле (1).
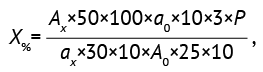 (1)
(1)
где Аx — оптическая плотность исследуемого раствора при длине волны 400±2 нм; А0 — оптическая плотность CO холин-хлорида при длине волны 400±2 нм; aх — навеска лекарственного препарата, г; a0 — навеска CO холин-хлорида, г; P — содержание холин-хлорида в СО, 98%.
Приготовление раствора соли Рейнеке. Около 1,5 г кристаллической соли Рейнеке растворяли в 80 мл воды очищенной, доводили полученный раствор до pH 1 по универсальному индикатору 2 М раствором кислоты хлористоводородной, фильтровали в мерную колбу вместимостью 100 мл и доводили объем раствора до метки водой очищенной.
Валидацию методики количественного определения холина проводили по следующим показателям: специфичность, линейность, правильность, прецизионность в соответствии с требованиями OФС.1.1.0012 Валидация аналитических методик (Государственная фармакопея Российской Федерации XV изд.).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Качественное определение азотистых оснований. На хроматограммах образца ушных капель при использовании системы растворителей: н-бутанол — этанол — уксусная кислота — вода (8:2:1:3) фиксируются четыре зоны адсорбции, имеющие темно-оранжевую окраску, которые можно отнести к зонам адсорбции азотистых оснований. При сравнении экспериментальных факторов удерживания с данными литературы идентифицированы холин, ацетилхолин, йодид ацетилхолина и бензоилхолин2 (табл. 1), также имеется одна размытая зона адсорбции. Наилучшее разделение наблюдалось при использовании системы растворителей н-бутанол — этанол — уксусная кислота — вода (8:2:1:3), поэтому для подтверждения наличия азотистых оснований в анализируемых ушных каплях использовали эту систему растворителей.
Таблица 1. Результаты анализа методом тонкослойной хроматографии образца капель ушных на основе омелы белой листьев экстракта густого
Table 1. Results of thin-layer chromatography of a sample of ear drops based on the Viscum album L. leaf soft extract
|
Значение факторов удерживания Retention factor values |
Обнаруженные холин и его сложные эфиры Choline and choline esters detected |
|
|
ушных капель ear drops |
стандартных образцов* reference samples* |
|
|
0,37±0,01 0,49±0,02 0,60±0,00 0,70±0,02 |
0,37 0,47 0,58 0,70 |
холин / choline ацетилхолин / acetylcholine йодид ацетилхолина / acetylcholine iodide бензоилхолин / benzoylcholine |
Таблица составлена авторами / The table is prepared by the authors
* Данные получены из: Хайс ИМ, Мацек К, ред. Хроматография на бумаге. М.: Издательство иностранной литературы; 1962.
* The data are obtained from Hayes I., Matzek K., Paper chromatography. Moscow, IL, 1962, 852 p.
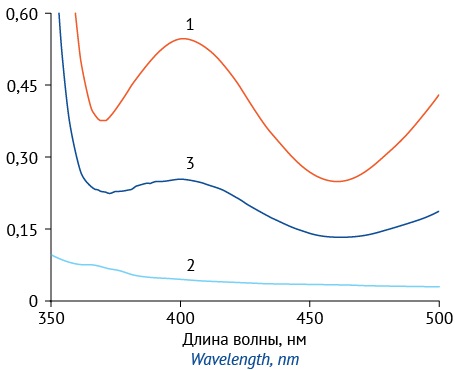
Рисунок подготовлен авторами по собственным данным / The figure is prepared by the author using their own data
Рис. 1. УФ-спектры ацетоновых растворов с добавкой соли Рейнеке: 1 — стандартный образец холин-хлорида; 2 — модельная смесь капель ушных без омелы белой листьев экстракта густого; 3 — капли ушные, содержащие омелы белой листьев экстракта густого
Fig. 1. UV spectra of acetone solutions of choline chloride (1), ear drops without V. album leaf soft extract (2), and ear drops with V. album leaf soft extract (3) with the addition of Reinecke’s salt
Валидация методики количественного определения сложных эфиров холина
Специфичность. Установлено, что максимум поглощения растворов образцов капель ушных, содержащих омелы белой листьев экстракта густого, в присутствии соли Рейнеке находится при 400±2 нм и совпадает с максимумом поглощения комплекса СО холин-хлорида с солью Рейнеке (I), а раствор модельной смеси лекарственной формы, не содержащей холин, имеет неизбирательное поглощение в анализируемом диапазоне (рис. 1). Таким образом, данная методика определения количественного содержания азотистых оснований специфична.
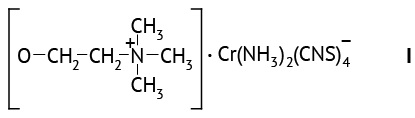
Линейность методики устанавливали, используя пять растворов анализируемых ушных капель различной концентрации (в диапазоне 0,100– 0,200 мг/мл). Мерой линейности служил коэффициент корреляции ≥0,99. Количественное соотношение объема пробы анализируемой лекарственной формы и раствора соли Рейнеке, приготовленных по методике, представленной выше, составляет 1:1,5. Уравнение зависимости оптической плотности от концентрации холина в анализируемых растворах представляет собой прямую (y=1,56x+0,0136) с высоким коэффициентом корреляции (R²=0,9961), что подтверждает линейность методики в диапазоне концентраций от 0,100 до 0,200 мг/мл.
Точность (правильность). В качестве исходного раствора использовали исследуемый раствор лекарственной формы с концентрацией, соответствующей верхнему пределу линейности методики (0,200 мг/мл). Из этого раствора готовили разведения в соотношении 1:2; 1:1; 1:0,5. На каждом уровне концентраций рассчитывали открываемость. На каждом уровне концентраций (1:2; 1:1; 1:0,5) получены сопоставимые результаты при относительном стандартном отклонении (RSD) 2,267% и стандартном отклонении (SD) 2,265%.
Прецизионность. Готовили шесть испытуемых растворов исследуемых ушных капель 25 мл (0,150 мг/мл). Результаты характеризуются удовлетворительной сходимостью с относительным стандартным отклонением результатов 3,03%.
С использованием разработанной методики было определено содержание холина в каплях ушных на основе омелы белой листьев экстракта густого, 0,710±0,018%.
ЗАКЛЮЧЕНИЕ
Разработана и валидирована методика количественного определения содержания сложных эфиров холина в пересчете на холин в ушных каплях церуменолитического действия на основе омелы белой листьев экстракта густого, основанная на спектрофотометрическом определении в присутствии соли Рейнеке при длине волны 400±2 нм.
С использованием разработанной методики определено содержание идентифицированных холина и его сложных эфиров в каплях ушных на основе омелы белой листьев экстракта густого в количестве 0,710±0,018%.
Вклад авторов. Все авторы подтверждают соответствие своего авторства критериям ICMJE. Вклад авторов распределен следующим образом: С.Л. Аджиахметова — проведение эксперимента, написание текста рукописи, статистическая обработка данных, формулировка заключения; А.Е. Позднякова — написание текста рукописи, участие в формулировании выводов, работа с источниками литературы, утверждение окончательной версии рукописи для публикации.
Authors’ contributions. All the authors confirm that they meet the ICMJE criteria for authorship. The most significant contributions were as follows. Similla L. Adzhiakhmetova conducted the experiment, drafted the manuscript, performed statistical data processing, and formulated the conclusions. Anastasiya E. Pozdnyakova drafted the manuscript, formulated the conclusions, worked with references, and approved the final version of the manuscript for publication.
1. Хайс ИМ, Мацек К, ред. Хроматография на бумаге. М.: Издательство иностранной литературы; 1962.
2. Хайс ИМ, Мацек К, ред. Хроматография на бумаге. М.: Издательство иностранной литературы; 1962.
Список литературы
1. Horton GA, Simpson MTW, Beyea MM, Beyea JA. Cerumen management: An updated clinical review and evidence-based approach for primary care physicians. J Prim Care Community Health. 2020:11:2150132720904181. https://doi.org/10.1177/2150132720904181
2. Roeser RJ, Ballachanda BB. Physiology, pathophysiology, and anthropology/epidemiology of human earcanal secretions. J Am Acad Audiol. 1997;8(6):391–400. PMID: 9433685
3. Clegg AJ, Loveman E, Gospodarevskaya E, Harris P, Bird A, Bryant J, et al. The safety and effectiveness of different methods of earwax removal: A systematic review and economic evaluation. Health Technol Assess. 2010;14(28):1–192. https://doi.org/10.3310/hta14280
4. Schwartz SR, Magit AE, Rosenfeld RM, Ballachanda BB, Hackell JM, Krouse HJ, et al. Clinical practice guideline (update): earwax (cerumen impaction). Otolaryngol Head Neck Surg. 2017;156:1–29. https://doi.org/10.1177/0194599817725542
5. Aaron K, Cooper TE, Warner L, Burton MJ. Ear drops for the removal of ear wax. Cochrane Database Syst Rev. 2018;7(7):CD012171. https://doi.org/10.1002/14651858.CD012171.pub2
6. Позднякова АЕ, Аджиахметова СЛ, Сергеева ЕО, Поздняков ДИ, Юртаева ЕА, Бородина ИО, Компанцев ДВ. Разработка состава и технологии капель ушных церуменолитического действия на основе омелы белой листьев экстракта густого. Фармация и фармакология. 2023;11(6):482–93. https://doi.org/10.19163/2307-9266-2023-11-6-482-493
7. Поздняков ДИ, Аджиахметова СЛ, Червонная НМ, Оганесян СО. Сравнительное изучение фенольного состава и антиоксидантной активности полупаразита Viscum album L. и листьев растений — хозяев Malus domestica Borkh., Pyrus communis L. Химия растительного сырья. 2023;(1):287–96. https://doi.org/10.14258/jcprm.20230110947
8. Pozdnyakov DI, Adzhiakhmetova SL, Popova OI, Oganesyan ET. Choline accumulation in mistletoe leaves (Viscum album L.) and the effect of extracts based on them on the course of the sporadic form of Alzheimer’s disease in experimental animals. Arab J Med Aromat Plants. 2023;9(1):1–22. https://doi.org/10.48347/IMIST.PRSM/ajmap-v9i1.33916
9. Бубенчикова ВН, Степнова ИВ. Изучение азотсодержащих соединений горлюхи ястребинковой (Picris hieracioides L.). Международный журнал прикладных и фундаментальных исследований. 2016;(11–6):1133–5. EDN: XBVUYZ
10. Гусев НФ, Петрова ГВ, Докучаева ЮА, Немерешина ОН. Содержание холина в растениях земляники зеленой южного предуралья. Известия Оренбургского государственного аграрного университета. 2013;(1):221–4. EDN: PWNXJR
11. Муравьева ДА, Попова ОИ, Вартанян КО. Азотистые основания омелы белой и формианы простой. Фармация. 1991;40(1):16–7. EDN: YNDSOH
12. Позднякова ТА, Бубенчиков РА. Изучение азотсодержащих соединений герани болотной. Вопросы биологической, медицинской и фармацевтической химии. 2015;(11):37–9. EDN: WFRPOV
Об авторах
С. Л. АджиахметоваРоссия
Аджиахметова Симилла Леонтьевна, канд. фарм. наук
пр. Калинина, д. 11, Пятигорск, 357532
А. Е. Позднякова
Россия
Позднякова Анастасия Евгеньевна, канд. фарм. наук
пр. Калинина, д. 11, Пятигорск, 357532
Дополнительные файлы
Рецензия
Для цитирования:
Аджиахметова С.Л., Позднякова А.Е. Разработка методики количественного определения холина в каплях ушных на основе омелы белой листьев экстракта густого. Регуляторные исследования и экспертиза лекарственных средств. 2025;15(1):57-62. https://doi.org/10.30895/1991-2919-2025-668
For citation:
Adzhiakhmetova S.L., Pozdnyakova A.E. Development of an Analytical Procedure for the Quantitative Determination of Choline in Ear Drops Based on Viscum album Leaf Soft Extract. Regulatory Research and Medicine Evaluation. 2025;15(1):57-62. (In Russ.) https://doi.org/10.30895/1991-2919-2025-668



































